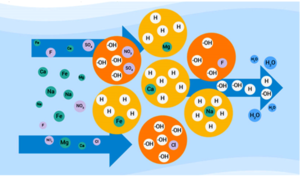
탈이온화는 전기를 띤 입자 또는 전리될 수 있는 유기질과 무기질 염이 용액으로부터 제거되는 공정이다.
이온에는 양이온과 음이온이 있다. 양이온은 양전하를 가진 이온으로서 나트륨(Na⁺), 칼슘(Ca⁺⁺), 마그네슘(Mg⁺⁺) 등이 여기에 포함된다. 음이온은 음전하를 가진 이온으로서 염소(Cl⁻), 황산(SO₄⁻⁻), 중탄산염(HCO₃⁻) 등이 여기에 포함된다.
물에서 이온을 제거하기 위해서는 물이 이온교환수지상을 통과할 때 발생하는 화학적 반응을 이용한다. 이 반응을 통해 수소 이온(H⁺)이 양전하 수지 표면의 양전하 이온과 교환되고 산화수고 이온(OH⁻)이 음전하 수지 표면의 음전하 이온과 교환된다. 이렇게 교환되는 H⁺와 OH⁻가 물 분자를 구성하는 원자들이다.[1]
탈이온수
탈이온수는 주로 DI water라는 이름으로 불리는데, 전기화학적 방법으로 만들어진다. 구체적으로는 전기적으로 하전된 수지, 즉 양전하 및 음전하를 띄는 이온교환수지에 수돗물 또는 증류수를 흐르게 하여 만들어진다. 이 과정을 통해 양이온 및 음이온은 이온교환수지에서 H⁺ 및 OH⁻와 교환하고 최종적으로 H₂O가 생성된다.
탈이온수는 물 내부에 이온이 존재하지 않아 반응성이 높다. 이로 인해 탈이온수는 공기에 노출되면 공기 중의 이산화탄소가 용해되기 시작하며 H⁺ 및 HCO₃⁻ 이온이 형성되고 pH가 7 미만으로 낮아져 산성을 띤다. 탈이온화 과정에서는 전기적으로 하전된 이온을 제거하는 공정이기 때문에 하전되지 않은 박테리아나 바이러스와 같은 유기 입자 또는 설탕과 같은 중성의 분자는 제거되지 않고 통과된다.[2]
각주
참고자료
같이 보기
|
  이 탈이온화 문서는 전기에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요. 이 탈이온화 문서는 전기에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요.
|
| 산업 : 산업, 산업혁명, 기술, 제조, 기계, 전자제품, 정보통신, 반도체, 화학, 바이오, 건설, 유통, 서비스, 에너지, 전기 □■⊕, 소재, 원소, 환경, 직업, 화폐, 금융, 금융사, 부동산, 부동산 거래, 부동산 정책, 아파트, 건물, 토지
|
|
|
| 전기
|
110V • 220V • 3상 • kW • kWh • 가변 전압 가변 주파수 제어 • 감전 • 강압 • 고전압 • 과부하 • 과전류 • 과전압 • 과충전 • 광자 • 교류(AC) • 극 • 기전력 • 나침반 • 누전 • 다이노드 • 다이오드 • 단락 • 단상 • 단자 • 단전 • 도선 • 도전율 • 도통 • 레독스 • 마찰전기 • 맥스웰 방정식 • 발전 • 발전기 • 방전 • 배전 • 번개 • 변압 • 변압기 • 변전 • 병렬 • 복합전극 • 볼트(V) • 부하 • 분산전원 • 비상전원 • 비저항 • 산화 • 산화반응 • 산화수 • 산화환원 • 산화환원반응 • 상용전원 • 소자 • 송전 • 송전선 • 송전탑 • 스파크 • 승압 • 승압기 • 암페어(A) • 애노드 • 양 • 양공 • 양극 • 양극단자 • 양극도선 • 양성자 • 양이온 • 양전기 • 양전자 • 양전하 • 영구자석 • 예비전원 • 옴(Ω) • 옴의 법칙 • 와트(W) • 와트시(Wh) • 원자 • 원자량 • 원자핵 • 웨버 • 유전상수 • 유전율 • 유전체 • 음 • 음극 • 음극단자 • 음극도선 • 음양 • 음이온 • 음전기 • 음전하 • 이온 • 이온전도 • 이온전도도 • 이온화 • 인력 • 자기 • 자기력 • 자기장 • 자석 • 자성 • 자속 • 자유전자 • 장 • 저전압 • 저항 • 저항기 • 전구 • 전극 • 전기 • 전기공학 • 전기력 • 전기분해 • 전기장 • 전기장치 • 전기저항 • 전기전도 • 전기전도도 • 전기회로 • 전도성 • 전도율 • 전도체 • 전동 • 전동화 • 전력 • 전력밀도 • 전류 • 전비 • 전선 • 전압 • 전원 • 전위 • 전위차 • 전자 • 전자계 • 전자기 • 전자기력 • 전자기장 • 전자기파 • 전자기학 • 전자석 • 전자파 • 전자회로 • 전하 • 전하량 • 절연 • 절전 • 점전하 • 정격전류 • 정격전압 • 정격출력 • 정전 • 정전기 • 주파수 • 중성미자 • 중성자 • 직렬 • 직류(DC) • 척력 • 초전도 • 초전도자석 • 초전도체 • 축전 • 출력 • 충방전 • 충전 • 캐소드 • 쿨롱 • 쿨롱의 법칙 • 킬로와트(kW) • 킬로와트시(kWh) • 탈이온화 • 터미널 • 테슬라 • 특고압 • 패러데이 법칙 • 하전 • 핵력 • 핵자 • 헤르츠(㎐) • 환원 • 환원반응
|
|
|
| 위키 : 자동차, 교통, 지역, 지도, 산업, 기업, 단체, 업무, 생활, 쇼핑, 블록체인, 암호화폐, 인공지능, 개발, 인물, 행사, 일반
|
|

 위키원
위키원