|
|
| 1번째 줄: |
1번째 줄: |
| − | [[파일:염화수소의 화학구조.jpg|썸네일|300픽셀|염화수소의 화학구조]] | + | [[파일:염화수소 화학구조.jpg|썸네일|300픽셀|염화수소의 화학구조]] |
| | '''염화수소'''(hydrogen chloride, 화학식: HCl)는 상온, 상압에서 자극적인 냄새가 나는 무색의 유독 [[기체]]이다. 염화수소 [[수용액]]은 [[염산]]이며 가장 널리 이용되는 강한 산(酸) 중의 하나이다. | | '''염화수소'''(hydrogen chloride, 화학식: HCl)는 상온, 상압에서 자극적인 냄새가 나는 무색의 유독 [[기체]]이다. 염화수소 [[수용액]]은 [[염산]]이며 가장 널리 이용되는 강한 산(酸) 중의 하나이다. |
| | | | |
2021년 11월 24일 (수) 15:26 판
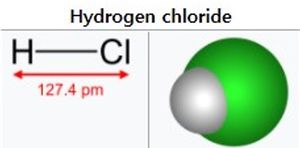
염화수소(hydrogen chloride, 화학식: HCl)는 상온, 상압에서 자극적인 냄새가 나는 무색의 유독 기체이다. 염화수소 수용액은 염산이며 가장 널리 이용되는 강한 산(酸) 중의 하나이다.
물리적 성질
- 화학식: HCl
- 분자량: 36.46g/mol
- 녹는점: -114℃
- 끓는점: -84℃
- 비중: 1.268 (기체)
- 비열용량: 0.7981J/(g·K)
- 용해도: 720g/L (20℃)
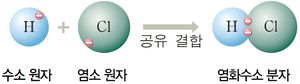
염화수소는 염소 원자와 수소 원자가 공유 결합한 화합물이다. 염소 원자의 전기음성도는 수소보다 훨씬 크기에 염화수소 분자는 강한 극성을 띄게 된다.
염화수소는 물에 잘 용해되며 부피로 500배, 무게로는 100g(20°C)의 물에 72g 녹는다. 알코올·에테르·벤젠 등 유기용매에도 잘 녹는다.
염화수소는 산의 특성을 강하게 지니므로, 인체에 매우 유해하며 습한 환경에서는 습기에 염화수소가 녹아 염산이 생성될 수 있으므로 주의해야 한다.
제법
공업적으로는 염소와 수소를 반응시켜 만들며, 각종 탄화수소를 염소화할 때 부산물로도 얻고 있다. 실험실에서는 진한 황산에 진한 염산을 떨어뜨려 발생시키거나, 식염과 진한 황산을 반응시켜서 만든다.
만하임 공법: 염화나트륨과 진한 황산을 반응시켜서 만드는 방법이다.
2NaCl + H₂SO₄ → Na₂SO₄ + 2HCl
직접 반응: 염화나트륨 수용액을 전기분해하여 수소와 염소를 생성한 다음 이를 직접 반응시켜서 염화수소를 생성하는 방법이다.
H₂ + Cl₂ = 2HCl
유기적 합성: 테플론, 프레온, PVC 등 염소가 들어있는 유기화합물을 이용해서 염산을 제조하는 방법이다.
고순도 HCl
고순도 HCl은 반도체 웨이퍼를 세정하거나 웨이퍼를 깎는 식각 공정에서 식각액으로 사용되는 소재이다. 삼성전자가 한국 내 HCl 수요의 약 80%를 소비할 정도로 반도체 산업 사용량이 압도적이다.
그러나 고순도 HCl은 대부분 해외에 의존하며 일본 화학업체 토아고세이와 독일 산업 가스 전문업체 린데가 과점 공급했다.
국산화 필요성이 커지고 일본의 반도체·디스플레이 소재 수출 규제 이후 공급망 재편이 화두로 떠오르면서 삼성전자와 백광산업 협력이 빠르게 진행되여, 생산 준비까지 끝낸 상황이다. [1]
용도
액상 염화수소 무수물은 염화비닐의 원료나 염산으로 사용된다.
각주
참고자료
같이 보기
|
  이 염화수소 문서는 소재에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요. 이 염화수소 문서는 소재에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요.
|
| 산업 : 산업, 산업혁명, 기술, 제조, 기계, 전자제품, 정보통신, 반도체, 화학, 바이오, 건설, 유통, 서비스, 에너지, 전기, 소재 □■⊕, 원소, 환경, 직업, 화폐, 금융, 금융사, 부동산, 부동산 거래, 부동산 정책, 아파트, 건물, 토지
|
|
|
| 소재
|
감광재 • 경화제 • 그래핀볼 • 그리스 • 금박 • 금속 • 금속재료 • 기름 • 나노소재 • 나프타 • 내화재 • 단열재 • 단일소재 • 도금 • 도전재 • 도체 • 동박 • 마감재 • 마찰재 • 막 • 매질 • 메타물질 • 무기재료 • 바닥재 • 박막 • 반도체 • 방부제 • 방음재 • 방진재 • 방청제 • 벽지 • 보강재 • 보온재 • 복합동박 • 복합소재 • 부도체 • 부산물 • 부식 • 부자재 • 불순물 • 살균제 • 소재 • 쇠붙이 • 수용액 • 시료 • 신소재 • 알루미늄 호일 • 에어로겔 • 엑소일렉트로겐 • 연마재 • 외장재 • 용매 • 용액 • 용융염 • 용질 • 원료 • 원소재 • 원자재 • 원재료 • 유기재료 • 유체 • 윤활유(윤활제) • 융해 • 은박 • 은박지 • 잉곳 • 자성체 • 자원 • 자재 • 재료 • 재질 • 전고체 • 전구체 • 절연체 • 접착제 • 접합재 • 접합제 • 제진재 • 주괴 • 중간재 • 증기 • 증착 • 차음재 • 천연소재 • 천연자원 • 천장재 • 철스크랩 • 첨가제 • 첨단소재 • 초전도체 • 촉매 • 컴파운드 • 코르크 • 코팅 • 쿠킹호일 • 탄소소재 • 페인트 • 포장재 • 폭발물 • 피복 • 피복재 • 호일(포일) • 흡음재
|
|
|
| 암석
|
각섬암(곱돌) • 간석기(마제석기) • 감람석 • 곡옥 • 골재 • 광물 • 광석 • 구리(동) • 규산염 • 규암(차돌) • 금 • 녹색편암 • 다이아몬드 • 대리석(대리암) • 돌 • 돌멩이 • 뗀석기(타제석기) • 루비 • 마그마 • 머드 • 모래 • 무쇠(주철) • 무연탄 • 바위 • 반려암 • 방해석 • 백금 • 백운암 • 벽돌 • 변성암 • 보석 • 비취 • 사암 • 사장석 • 사파이어 • 석고 • 석기 • 석영(수정, 쿼츠) • 석재 • 석탄 • 석회 • 석회암(석회석) • 섬록암 • 세라믹 • 셰일(혈암) • 쇠 • 수성암 • 스테인리스강 • 스피넬(첨정석) • 슬래그 • 시멘트 • 심성암 • 아메트린 • 아스콘 • 암석 • 암편 • 에메랄드 • 역암 • 역청탄 • 오석 • 오일셰일(함유셰일, 유혈암) • 오팔 • 옥 • 용암 • 운모 • 운석 • 원료탄 • 원석 • 유리 • 은 • 응회암 • 이암 • 이판암 • 인공 다이아몬드 • 인광석 • 자갈 • 자수정 • 잔석기 • 장석 • 점토(찰흙) • 점판암 • 정장석 • 조암광물 • 조흔색 • 종유석 • 준광물 • 지르콘 • 지하자원 • 진흙 • 천연암석 • 철광석 • 철기 • 철재 • 청금석 • 청동기 • 콘크리트 • 큐빅 • 토사 • 토파즈 • 퇴적암 • 편마암 • 편암 • 현무암 • 혼펠스 • 화강암 • 화산암 • 화성암 • 황철석 • 휘석 • 흑요석 • 흙 • 희토류
|
|
|
| 섬유
|
가죽 • 거위털(구스다운) • 거즈 • 고급가죽 • 고무줄 • 광목 • 광물섬유 • 광섬유 • 극세사 • 금속섬유 • 기모 • 깃털 • 끈 • 나노셀룰로스 • 나일론 • 나파가죽 • 낙타털 • 네오프렌 • 노르디코 • 누비 • 능직 • 다기능성 탄소나노튜브 섬유 • 다운 • 대마 • 데님 • 동물섬유 • 돼지가죽 • 라이오셀(리오셀) • 레이온(인견) • 리넨(린넨) • 마 • 마닐라삼 • 마닐라지 • 마분지 • 말가죽 • 메쉬 • 면 • 면직물 • 면화 • 명주 • 모 • 모다크릴 섬유 • 모달 • 모시 • 모직물 • 모피 • 목재 • 목화 • 무기섬유 • 무명 • 밍크털 • 반합성섬유 • 밧줄 • 방모 • 방모사 • 방모직물 • 방적 • 방직 • 방직섬유 • 뱀가죽 • 벨로아 • 벨벳 • 벨보아 • 보풀 • 부직포 • 붕소섬유 • 비건가죽 • 비단(실크) • 비스코스 • 삼베 • 새끼줄 • 석고보드 • 석면 • 석영섬유 • 섬유 • 세라믹섬유 • 셀룰로스 • 소가죽 • 소모 • 소모사 • 소모직물 • 솜 • 솜털 • 수자직(주자직) • 순모 • 슈퍼섬유 • 스웨이드(세무) • 스판덱스 • 시어서커 • 식물섬유 • 실 • 실리카섬유 • 아라미드 • 아세테이트 섬유 • 아크릴 섬유 • 악어가죽 • 알칸타라 • 암면 • 양가죽 • 양모 • 양모사 • 양모직물 • 오리털(덕다운) • 옷감 • 우레탄 • 울 • 원단 • 원모 • 원목 • 원사 • 유기섬유 • 유리섬유 • 인조가죽 • 잔털 • 재생섬유 • 종이 • 직물 • 짚 • 천 • 천연가죽 • 천연섬유 • 천연펄프 • 캐시미어 • 코듀로이(골덴) • 타조가죽 • 탄소섬유 • 탄화규소섬유 • 털 • 털실 • 텐셀 • 토끼털 • 패브리칸 • 펄프 • 평직 • 프로믹스 • 플란넬 • 플리스(폴라폴리스) • 피혁 • 합성섬유 • 합판 • 혼방 • 화학섬유(인조섬유)
|
|
|
수지
(플라스틱)
|
ABS • EVA • PVC • 고무 • 공중합체 • 라텍스 • 레진 • 모노머 • 목타르 • 바이오플라스틱 • 본드 • 부틸 • 부틸고무 • 부틸테이프 • 비닐 • 비닐기 • 비닐론(비날론) • 생고무 • 생분해성 플라스틱 • 송진 • 수액 • 수지 • 스티로폼 • 스펀지 • 시트 몰딩 컴파운드(SMC) • 실리콘 • 아스팔트 • 아크릴 • 에폭시 • 엔지니어링 플라스틱 • 염화비닐 • 천연고무 • 천연수지 • 콜타르 • 타르 • 페놀수지 • 페트(PET, 폴리에틸렌 테레프탈레이트) • 페트병 • 포지드 카본 • 폴리머(중합체) • 폴리비닐알코올 • 폴리실리콘 • 폴리아미드 필름 • 폴리아크릴 • 폴리아크릴로나이트릴 • 폴리에스테르(폴리에스터) • 폴리에틸렌 • 폴리염화비닐 • 폴리염화비닐라이덴 • 폴리올레핀 • 폴리우레탄 • 폴리카보네이트 • 폴리프로필렌 • 플라스틱 • 필름 • 합성고무 • 합성수지 • 호박
|
|
|
| 위키 : 자동차, 교통, 지역, 지도, 산업, 기업, 단체, 업무, 생활, 쇼핑, 블록체인, 암호화폐, 인공지능, 개발, 인물, 행사, 일반
|
|

 위키원
위키원