항체

항체(抗體, antibody, Ab) 또는 면역글로불린(immunoglobulin, Ig)은 항원과 특이적 결합을 하여 항원-항체 반응을 일으키는 물질이다. 혈액의 혈소판은 적혈구와 반응하여 응집하고 태어날 때부터 항상 가지고 있으므로 정상 항체 또는 동종 항체라 한다. 면역 체계에서 세균이나 바이러스같은 외부항원들과 특이적 결합을 하여 항원을 인식하게하고 동시에 무력화시키는 작용을 하는 면역글로불린은 면역 항체라고 하는데 보통 항체라고 하면 면역 항체를 뜻한다. 항체와 면역글로불린은 동일한 의미로서 면역글로불린은 항체로서 작용하는 당단백질이다. 여러 종류의 면역글로불린이 있는데 이들을 면역글로불린 상과(上科)(immunoglobulin superfamily)로 묶어 분류하고 있다. 항체는 혈액과 조직액뿐만 아니라 분비물(눈물 등)에서도 발견되는데 형질세포에서 생성, 분비된다. 형질세포는 면역계의 B세포가 T세포와의 상호작용하는 가운데 B세포가 특정 항원과 결합하여 분화된 세포이다. 각 항체는 특이적으로 항원과 결합하며 형질세포에 의한 항체의 생산은 체액성 면역이라고도 불린다.
목차
개요
항체는 면역글로불린 (Immunoglobulin: Ig)으로도 불리고 주로 형질B세포에서 생산되어 병원성 박테리아나 바이러스를 중화시키는 기능 등을 수행한다. 항체는 형질면역반응을 담당하는 주역이고, 병원균 고유의 특징적 분자 즉, 항원을 Fab(항원결합 조각, 아래그림1의 1)의 변이 부위 (Variable region: V)를 통하여 인식한다. 항체가 인식하는 항원의 부위를 항체인식부위 (epitope)라 한다. 항체는 항원에 결합하여 (가령, 박테리아나 바이러스가 감염하거나 생존하는데 필수적인 분자에 결합하여) 중화시키거나 (즉, 필수 분자들의 기능을 억제함으로써), 이들 또는 이들에 의해 감염된 세포를 표지함으로써 면역계의 다른 요소들이 공격할 수 있도록 유도한다. 항체가 면역계의 다른 요소들과 교통하여 면역기능을 나타내는 것은 Fc 부위를 통하여 이루어지며 (아래그림1의 2), 이 부위는 또한 항체의 종류를 결정한다.
항체는 적응성 면역계의 B세포, 특히 대부분은 분화된 형질세포에 의해서 분비된다. 항체는 분비되어 혈액 내의 혈장에 자유롭게 돌아다니는 분비형과 B 세포의 표면에 수용체 형태(B세포수용체)로 발현되는 막형의 두 가지 형태로 만들어진다. B세포수용체(B cell receptor: BCR)는 B세포의 표면에서만 발견되며 이들 세포의 활성화를 매개하고 이에 따른 세포의 형질세포 또는 기억세포로의 분화를 촉진한다. 형질세포가 생산하는 항체는 막형의 B세포수용체와 동일한 Fab 부위를 가지고 있어 같은 항원 부위를 인식하나, Fc 부위는 막형이 아닌 분비형의 구조를 가짐으로써 B 세포수용체가 인식한 동일한 항원 부위에 대한 적절한 면역 기능을 나타내도록 한다. B세포가 항원을 인식하여 완전히 활성화되고 이에 따라 항체를 생산하는 대부분의 경우에는 B세포와 도움 T세포간의 상호작용을 필요로 한다.
발견
'항체'라는 용어가 처음 사용된 것은 독일의 과학자 파울 에를리히(Paul Ehrlich)의 논문에서 쓰인 'Antikörper'이지만, 항체라는 물질이 혈청에 존재한다는 획기적인 사실이 처음 알려진 것은 1890년에 이루어진 에밀 아돌프 폰 베링(Emil Adolf von Behring)과 키타사토 시바사부로(Shibasaburo Kitasato)의 연구이다. 이 두 과학자는 파상풍균을 이용한 실험에서 독성이 약화된 파상풍균에 걸린 적 있는 토끼의 혈청을 주사받은 마우스들은 이후 독성이 약화되지 않은 생독성 파상풍균에 감염되어도 멀쩡하다는 사실을 발견했다. 이 발견으로 베링은 1901년에 첫 노벨생리의학상을 수상하는 영예를 누렸다. 이 발견이 매우 중요했던 것은 두 가지 측면에서 설명할 수 있다. 첫째로는, 병원체에 감염된 생물은 혈청에 그 병원체를 막을 수 있는 물질을 생산한다는 점이다. 둘째는, 그렇게 형성된 물질은 혈청을 통해 다른 개체에게 전달될 수 있다는 점이다. 이런 발견은 오늘날 수많은 인명을 구했고, 또 구하고 있는 예방접종 개념의 기초가 되었다는 점에서 매우 중요하다.
항체의 구조
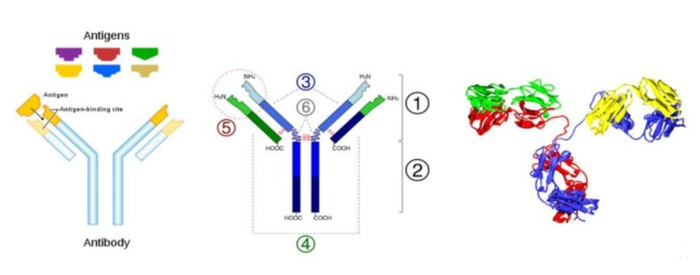
기본 구조는 Y자형의 단백질이며, Y자의 위쪽 두 가지에 항원과 결합할 수 있는 특이적 구조를 가지고 있다. 이러한 특이적 구조는 면역 세포에서 일어나는 DNA 수준에서의 유전자 재배열에 의해 상상할 수 없을 정도로 많은 가짓수를 가질 수 있으므로, 다양한 항원에 대응할 수 있다.
항체는 비교적 큰 분자량을 가진 단백질로서 아미노산기에 당사슬이 결합하고 있다. 대부분의 면역글로불린 상과(上科) 항체들은 아미노산의 N-말단에 결합하고 있지만 IgA1와 IgD 경우만 O-말단에 결합하고 있다. 각 항체의 기본 단위는 각각 경사슬 2개와 중사슬 2개가 이황화 결합을 하여 이루어진 Y자 모양을 한 단량체 분자이며 단량체가 1- 5개까지 모여 하나의 항체를 구성한다.
중사슬 (heavy chain)
5가지(γ, δ, α, μ, ε) 종류가 있으며 중사슬이 항체의 종류를 결정짓는다. α와 γ는 450개, μ와 ε는 550개의 아미노산으로 구성되어 있다. 중사슬에는 두 영역 즉 가변 영역과 불변 영역이 있다. 가변 영역은 항체가 만들어지는 B세포(형질 세포)에 따라 달라지며 같은 세포에서 만들어지는 항체의 가변영역은 모두 동일하다. 불변 영역은 항체의 종류가 같을 때만 동일하다. γ, α, δ는 3개의 불변 영역이 있고 구부러지는 영역을 가지고 있지만 μ, ε는 4개의 불변 영역을 가지고 있다. 모든 중사슬의 가변 영역은 한 군데만 있으며 110개 정도의 아미노산으로 구성되어 있다. 가변 영역은 아미노산으로 서로 연결된다.
경사슬 (light chain)
λ, κ 2가지 종류가 있으며 대략 211-217개의 아미노산으로 구성되어 있다. 사람의 항체 각각에는 모두 동일하게 1가지의 경사슬만이 존재한다. 경사슬은 불변 영역과 가변 영역이 연속적으로 이루어져있다.
Y모양의 항체 단량체는 2개의 중사슬과 2개의 경사슬이 모여 이루어져 있으며 6-8개의 불변 영역과 4개의 가변 영역을 가진다. 항체의 갈라진 부분(Y의 가지부분)을 Fab조각(Fab(fragment antigen binding) fragments)이라고 하는데 불변 영역과 가변 영역 각각 1개씩을 가지며 N-말단이 항원에 결합한다. 2개의 가변 영역이 특정한 항원에 결합하는 부위이다.
효소에 따라 항체를 자르는 부위가 다르기 때문에 서로 다른 효소를 이용하여 항체 구조를 연구하는 데 사용했는데 파파인효소와 펩신효소가 대표적이다. 파파인 효소는 항체 단량체를 2개의 Fab(fragment antigen binding)조각과 1개의 Fc (fragment crystallizable)조각으로 나눈다. 펩신은 항체를 접혀지는 부분 아래를 자르기 때문에 f(ab)2 조각 1개와 fc조각 1개로 나뉜다.
동형상
| 명칭 | 설명 | 항체 구조 |
| IgA | 장, 기도, 요도 등의 점막에 포함되어 있으며, 병원체에 의한 감염을 방지한다. 침, 눈물, 모유 등에도 포함되어 있다. | 
|
| IgD | 주로 항원에 노출되지 않은 B 세포의 항원 수용체로 작용한다. 호염기성 백혈구와 비만세포를 활성화시켜 항균 물질이 생산되도록 한다. | |
| IgE | 알레르겐과 결합하여 비만 세포와 호염기성 백혈구로부터의 히스타민 분비를 촉진한다. 이는 알레르기를 유발한다. 기생충 감염을 예방하는 역할도 한다. | |
| IgG | 항체의 대부분을 차지한다. 항체 중 유일하게 태반을 통과하여 태아에게 수동 면역을 형성한다. | |
| IgM | 충분한 양의 IgG가 생성되기 전의 단계에서 항원을 제거한다. |
항체의 무거운 사슬의 불변 영역의 차이에 따라 항체는 IgG, IgA, IgM, IgD, 그리고 IgE 5가지의 동형상으로 분류된다.
- Ig A : 몸의 점막 부분에 많이 존재한다. 최전선의 면역 반응을 담당하며, 외부 기생체의 침입을 방어한다. 혈청으로 분비 시 주로 단량체로 분비된다.
- Ig D : 신생 B세포의 세포막에 막관통형으로 발현되는 항체이다. 거의 연구되어 있지 않다.
- Ig E : 알러지 반응 및 염증 반응에서 주로 작용한다. 비만 세포와 결합하여 히스타민을 분비하게 한다. 비만세포와 호염구의 Fc 수용체에 결합한다.
- Ig G : 면역 반응을 주로 담당하는 항체. 면역 반응이 진행되면서 Ig M이 Ig G로 바뀌어 생산된다. 단량체로 분비되며, 혈액 내 가장 많이 존재한다. 2차 면역 반응에 의해 생산되는 주요 항체이다.
- Ig M : 면역 반응 시 최초로 만들어지는 항체. 다섯 개의 Y가지가 결합되어 있다. 오량체로 분비되며, 신생 B세포의 세포막에 막관통형으로 발현되는 항체이다.
- Ig Y : 조류에서 유래한 항체로서, 헬리코박터 증식 억제 등의 이유로 일부 식품에 첨가되는 항체.
기능
항체들이 수행하는 기능들은 다음과 같다.
- 중화(neutrilazation) - 병원체나 병원체가 분비하는 독소가 세포 내로 세포내이입(endocytosis)되는 것을 방지하며, 모든 클래스의 항체들이 가지는 기능이다.
- 응집(agglutination) - 단량체 항체는 2개의 항원 결합 부위를 가지므로, 항체는 여러 병원체에 동시에 결합하여 병원체들이 서로 뭉치게 하여 중화 작용이나 물리적인 제거가 쉽게 일어날 수 있게 하는데, 이를 응집 작용이라고 한다.
- 옵소닌화(opsonization) - 포식세포의 포식능을 강화시키는 작용이다. 항원 결합 부위가 항원에 결합하고 밑쪽의 Fc 부위는 포식세포 세포막의 수용체인 FcR에 결합하여 포식작용이 일어나기 쉽게 하며, 이런 식으로 일어나는 비정상 세포가 포식되는 포식작용은 항체의존성 세포포식작용(antibody-dependent cellular phagocytosis, ADCP)이라고 부른다.
- 보체의 활성화(complement activation) - 항원-항체 복합체(Ag-Ab complex; immune complex)는 보체 활성화가 일어나는 세 가지의 경로 중 보체활성화 고전경로가 일어나도록 한다. 고전경로가 활성화되어 보체의 기능이 활성화되면 막공격복합체(membrane attack complex, MAC)가 형성되어 병원체 세포막을 뚫고 용균(lysis)을 일으킨다.
- 항체의존성 세포매개독성(antibody-dependent cell-mediated cytoxicity, ADCC) - 항체가 비정상 세포가 세포막에 발현하는 외부(non-self) 항원에 결합하면, 그 항체(특히 사람에서는 IgG1)의 Fc 부위를 자연살해세포나 세포독성 T 세포와 같은 세포독성세포가 인식하여 비정상 세포의 세포자멸사(apoptosis)를 유발할 수 있다.
- 과립구의 탈과립(degranulation of granulocyte) - IgE 클래스 항체 등은 과립구가 세포 안에 가지고 있는 과립 성분들(주로 병원체를 죽이기 위한 용해 효소 등)을 분비하게 하여 병원체를 살상할 수 있다.
항체 형성
일반적으로 태어난 순간에는 모체에서 유래된 항체는 존재하지만 특정한 항원을 인식하지는 못한다. 성장하면서 각종 박테리아와 같은 미생물이나 바이러스 등에 노출되거나 병에 걸림으로 특정한 항원을 인식하게 된다. 초기 형태의 항체는 모두 B세포에 부착되어 있다. 이들을 B세포수용체(B cell receptor, BCR)라고 한다. 새로운 항원이 이 수용체와 결합하게 되면 항원에 노출된 적이 없는 B세포(native B cell)가 활성화되고 증식된다. 이때 대부분의 B세포는 대부분 형질세포(plasma cell)로 분화하지만, 일부 세포들은 기억 B세포(memory B cell)로 분화된다. B세포가 분화할 때 항원결합부위(paratope)를 구성하는 단백질의 유전자 서열이 무작위로 바뀌게 되면서 낮은 확률이지만 특정 항원을 인식할 수 있는 항체가 얻어지게 된다. 형질세포(plasma cell)는 혈액, 조직액(tissue fluid), 다양한 분비액에 용해되는 항체를 생성하여 항원을 제거한다. 기억B세포들은 오랫동안 또는 평생 체내에서 면역성을 유지한다.
의학적 응용
질병 진단
특정 항체를 검색하는 것은 일반적인 질병 진단 방법으로 이용된다. 항체의 특이적 결합 특성을 응용하여 ELISA, 면역 형광법, 면역 확산법, 면역 전기영동법, 웨스턴 블로팅 등의 방법으로 항체-항원 결합체를 탐지함으로 전염성 질병 감염 여부를 진단할 수 있다. 자가면역 질환(autoimmune disorder)도 자신 몸의 항원결정기(epitope)에 결합하는 항체를 발견함으로 진단할 수 있다.
항체 치료
항체 치료제라고 불리는 단일클론 항체(monoclonal antibody) 약물은 1986년 처음 FDA의 승인을 받고 시장에 나왔다. 단일클론 항체(monoclonal antibody)는 단 하나의 항원결정기에만 항체반응을 하는 특이성이 동일한 항체로서 유전자 재조합 기술의 발전으로 자가면역질환, 류마티즘, 암 등 다양한 질병 치료에 활용되고 있다.
장기이식거부반응을 줄이는 면역억제제는 면역계의 T세포의 활성을 약화시키고자 T세포 표면의 CD3 단백질을 항원으로 표적하여 항체 치료제가 T세포 표면에 달라붙어 연관 작용을 방해함으로 거부반응을 약화시킨다.
심장질환에 관련된 항체 치료제는 혈소판 응집에 관여하는 단백질을 항원으로 정하여 관상동맥의 혈전 생성을 억제하여 심장질환 위험성을 낮추게 한다.
항암제로 개발되는 항체 치료제는 암세포 표면에 특별히 존재하는 단백질을 항원으로 표적하여 이와 결합하는 항체를 이용하면 암세포의 증식을 막거나 면역세포를 불러들인다.
자가면역질환은 면역계 과잉 반응으로 자기 조직을 공격한다. 이 과정에 면역계의 세포 신호에 관여하는 TNF(종양괴사인자)와 같은 작은 단백질을 항원으로 하는 항체 치료제는 TNF 농도를 낮추어 증상을 줄이게 된다.
흑생종과 같은 피부암의 암세포는 T세포 표면의 PD-1과 결합해 T세포가 자신을 공격하지 않게 유도한다. 이때 항체 치료제가 먼저 PD-1에 달라붙게 하여 T세포가 자유롭게 암세포를 공격하게 한다.
항체약물접합체(antibody-drug-conjugate, ADC)
항체약물접합체(antibody-drug-conjugate, ADC)는 단일클론 항체에 약물을 연결시킨 복합체로서, 주로 암세포 표면이 발현하는 항원을 항체가 선별하여 인식 결합하여 암세포에 세포 독성 약물을 유도하도록 설계된 암 치료제로 개발되고 있다. 항체 및 약물은 세포에 의한 ADC의 내재화 및 소화 시 세포 독성 약물의 방출을 가능하게 하는 화학 결합을 통해 연결된다.
최초의 ADC 치료제는 철회되었다가 2017년 FDA에서 다시 승인된 미국 제약사인 화이자의 mylotarg로 급성골수성백혈병(acute lymphoblastic leukemia (ALL)) 치료제이다. 유전자 재조합으로 얻어진 IgG4 항체와 DNA 결합형 세포독성을 나타내는 칼리치마이신(calicheamicin) 유도체를 결합시킨 물질이다.
동영상
참고자료
같이 보기

 위키원
위키원