항생제
항생제(antibiotic) 또는 항균제 또는 항생물질(抗生物質)은 "미생물이 생산하였고 다른 미생물의 성장과 증식을 억제하는 물질"이라고 정의된다. 병원성 박테리아 감염의 치료 및 예방에 사용되는 항균제 약물이다. 통속적으로 항바이러스제와 혼동될 수도 있지만 잘못된 것이다. 이러한 물질로 만든 약을 항생제 또는 일상적으로 마이신(mycin)이라고 부른다. 항생제는 감기나 인플루엔자와 같은 바이러스에 효과적이지 않다. 바이러스를 억제하는 약물은 항생제가 아닌 항바이러스 약물 또는 항바이러스제라고 한다.
처음에는 곰팡이 또는 토양 미생물이 자연적으로 만들어 낸 것을 이용했으나, 현재는 구조를 약간 바꾼 반합성, 또는 완전히 새로운 합성 항생제도 많이 개발되어 사용되고 있다. 주로 결핵치료에 쓰이는 방선균(放線菌)의 하나인 스트렙토미세스속(屬)에서 분리한 항생 물질인 스트렙토마이신(streptomycin)에서 유래하여 '마이신'(mycin)으로 약칭하기도 하지만, 정확한 표현은 아니다. 영어 어원인 antibiotics는, 반대/저항이라는 뜻의 anti와 삶/살아있는 것을 뜻하는 bio의 결합으로, 미생물을 죽인다 혹은 저항한다는 뜻이다.
참고로, 항균제(antimicrobia)와 항생제(antibiotics)도 구별할 수 있다. 항균제는 비누와 소독제에 사용되며, 항생제는 의약품으로 사용된다.
목차
[숨기기]정의 및 명칭[편집]
항생제(抗生劑, antibiotics)란 다세포 생물의 생체조직 내에서 특정 세균의 증식이나 생존 활동을 중점적으로 방해하는 약물의 총칭이다.
- 'Antibiotic'이라는 단어는 1942년 S. A. Waksman이 최초로 학술지에 기술하였다. 일반적으로 항생제는 항균제(antibacterial agents)와 항미생물제제(antimicrobial agents)와 혼용되어 쓰이는데, 엄격히 말하면 두 단어는 항생제와는 다른 의미를 내포한다. 항균제는 인공적으로 합성 혹은 반합성한 약물을 일컬으며 세균(bacteria) 외에 작용하는 항진균제(antifungal agent), 항바이러스제(antiviral agent), 항원충제(antiprotozoal agent)는 포함하지 않아 이러한 의미를 내포하고자 할 때는 항미생물제제라는 표현이 권장된다.
- 《미생물학》, 한국미생물학회 저, 질병관리청에서 재인용
본래 항생제(antibiotics)는 미생물에 의해 만들어진 물질 가운데 다른 미생물, 특히 세균의 증식과 성장을 억제하는 효과가 있는 물질을 약물로써 사용하는 것만을 가리켰다. 최초의 항생제인 페니실린을 푸른곰팡이로부터 얻은 것이 그 예이다. 따라서 좁은 의미의 항생제를 가리킬 때 '인공적인 합성 물질'은 유사한 효과를 보이더라도 항생제에 포함되지 않는다.
그러나 근대 이후 빠른 속도로 의학이 발달함에 따라 인공적인 항균 물질 합성 개발도 활발해지게 됐다. 이에 의학자들은 인공적으로 합성 또는 반합성된 항균물질을 기존의 항생제와 비교하여 항균제(antibacterial agents)라고 칭했는데, 실무에서는 항생제와 항균제가 유사한 기능을 수행하도록 처방되었으므로 항생제와 항균제를 구분하지 않고 '항생제'라고 부르거나, 전자를 '천연 항생제'라고 부르는 용례가 확산되었다.
한편, 항균제의 '항균'은 세균(bacteria)에 대항하는 물질만을 가리키므로, 진균(곰팡이)이나 바이러스, 원충 등 다른 미생물에 작용하는 약제까지 항균제라고 하면 엄밀히 말해 틀린 것이 된다. 따라서 항진균제, 항바이러스제, 항원충제를 포괄하는 넓은 의미의 항생제는 항미생물제제(antimicrobial agents)라고 부르는 것이 권장된다.
또 항생제는 세균에 미치는 영향에 따라 세균의 성장과 번식을 억제하며 인체의 면역계가 함께 작용하도록 하는 정균성(bacteriostatic) 항생제와, 성장 중인 세균을 직접 죽이지만 증식하지 않는 휴지기 상태의 세균은 죽일 수 없는 살균성(bactericidal) 항생제로도 나뉜다.
한편 항생제를 '마이신(mycin)'이라고도 부르는데, 이는 결핵 치료에 쓰이는 스트렙토마이신(streptomycin)의 이름에서 유래한 별칭으로 이후 개발된 항생제, 특히 아미노글리코사이드계 항생제의 접미사로 쓰이고 있다. 이 밖에 '신(-cin)'을 접미사로 갖는 항생제도 있다.
기원[편집]
숙주인 사람에게는 해롭지 않고 병원체에게만 큰 손상(injury)을 미치는 물질로 감염병 환자를 치료하는 것을 화학요법이라고 한다. 그러나 이러한 요법이 실시된 것은 화학요법이란 말이 생기기보다 아득한 옛날이다. 즉 조충(tapeworm) 치료에 고사리의 일종인 malferin을, 회충증에는 santonin을, 말라리아에는 quinine을, 아메바감염증에는 emetine을 사용한 역사는 미생물학의 역사보다는 월등하게 앞선다.
전염병의 원인이 미생물에 의해 생긴다는 것이 로베르트 코흐와 루이 파스퇴르에 의해 알려지면서, 사람들은 병을 치료하기 위해 미생물을 죽이는 물질을 찾기 시작했다.
근대 화학요법은 파울 에를리히로부터 시작되었다고 해도 과언이 아니다. 에를리히는 조직염색표본에서 원충이 특이하게 염색된다는 사실로부터 염색약품이 원충과 특이한 친화성(affinity), 즉 선택독성이 있다는 사실에 착안하여 염료가 치료에 사용될 수 있으리라는 생각으로 염료를 연구하여 끝내는 1909년에 염료는 아니지만 살바르산(salvarsan)을 만들어 근대 화학요법의 선구자가 되었다.
최초의 항생제로서 매독 치료제인 살바르산은 세균 성장을 억제하는 작용을 한다. 또한, 페니실린은 최초로 만들어진 미생물을 직접 파괴하는 종류의 항생제이다.
작용[편집]
항균 방식[편집]
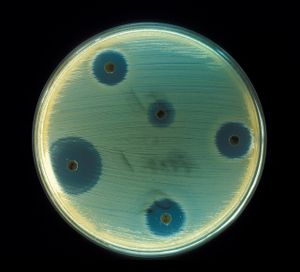
항생제는 종류에 따라 살균 작용과 정균 작용을 수행한다. 살균 작용(bactericidal effect)은 미생물을 직접 죽이는 것이고, 정균 작용(bacteriostatic effect)은 미생물이 더 이상 번식하지 못하도록 억제하는 것이다. 정균 항생제를 사용하는 경우 미생물은 결국 식균작용이나 항체 등 숙주의 방어기전에 의해 제거된다.
작용 범위[편집]
항생제마다 항균 스펙트럼이 다르다. 광범위항생제(broad spectrum antibiotic)는 다양한 그람양성균과 그람음성균에 효과를 나타내는 반면, 특정한 종류 미생물에 대해서만 효과를 나타내는 좁은범위항생제(narrow spectrum antibiotic)도 존재한다.
작용 기전[편집]
인체 감염을 치료하기 위해 항생물질을 이용하려면, 항생물질이 선택적 독성을 가져 병원체에 손상을 입히면서도 인간 세포에는 영향을 미치지 않아야 한다. 세균 등 원핵생물을 표적으로 하는 항생물질을 찾기는 비교적 쉬운데, 원핵생물과 진핵생물의 구조적·기능적 특징이 상당히 다르기 때문이다. 반면 곰팡이나 원생생물, 기생충처럼 진핵세포로 이루어진 병원체를 표적으로 하는 항생물질은 개발하기가 한결 어렵고 따라서 그 종류도 다소 한정적이다.
원핵세포와 항생물질[편집]
세균을 표적으로 하는 항생물질의 작용 기전과 그 대표적인 예시를 나열하면 다음과 같다.
- 세포벽 합성 억제 : 진핵생물과 달리 원핵생물의 세포는 세포막뿐만 아니라 펩티도글리칸으로 이루어진 세포벽을 갖는다. 따라서 세포벽은 세균에 대한 항생물질의 이상적인 표적이 된다. 페니실린, 세팔로스포린, 카바페넴, 모노박탐 등 베타-락탐 계열 항생제는 펩티도글리칸의 교차결합을 억제하여 세포벽 합성을 저해한다. 반코마이신 등 당펩티드 항생제 역세 세포벽을 표적으로 하는 항생물질에 해당한다.
- 단백질 합성 억제 : 80S 리보솜을 갖는 진핵생물과 달리 원핵생물은 70S 리보솜을 갖는다. 리보솜의 구조적 특징이 다르기 때문에, 세균의 리보솜에 작용하여 단백질 합성을 억제하는 항생물질은 선택적 독성을 나타낼 수 있다. 하지만 진핵생물의 중요한 세포 소기관인 미토콘드리아 역시 70S 리보솜을 갖기 때문에, 숙주세포에 유해한 부작용이 발생할 가능성을 배제할 수 없다. 대표적인 항생물질을 나열하면 다음과 같다.
- 아미노글리코사이드 계열 항생제 : 30S 소단위체가 mRNA를 인식하는 과정을 방해함으로써 살균작용을 나타낸다. 스트렙토마이신, 네오마이신, 아미카신, 카나마이신, 젠타마이신 등이 있다.
- 테트라사이클린 계열 항생제 : 30S 소단위체가 tRNA와 결합하는 과정을 억제한다. 테트라사이클린, 독시사이클린, 티게사이클린 등이 여기에 해당한다.
- 마크로라이드 계열 항생제 : 50S 소단위체의 23S rRNA에 결합하여 정균작용을 나타낸다. 합성 중인 폴리펩타이드 사슬이 리보솜으로부터 일찍 떨어져 나가도록 하거나 50S 소단위체의 조립을 방해하는 등 다양한 방식으로 단백질 합성을 억제하는 것으로 알려져 있다. 에리트로마이신, 아지트로마이신, 클래리트로마이신 등이 있다.
- 린코사마이드 계열 항생제 : 50S 소단위체에 결합하여 단백질 합성의 개시를 방해함으로써 정균작용을 나타낸다. 클린다마이신이 대표적이다.
- 옥사졸리디논 계열 항생제 : 반코마이신 내성균에 대응하기 위해 개발된 항생제로, 50S 소단위체에 작용하여 30S 소단위체와 결합하는 것을 억제한다. 리네졸리드가 대표적이다.
- 클로람페니콜 : 50S 소단위체의 23S rRNA에 결합하여 새로운 펩타이드 결합이 형성되는 것을 억제한다.
- 핵산 합성 억제 : 리팜핀 등 리파마이신 계열 항생제는 세균의 RNA 중합효소에 작용하여 mRNA 합성을 억제하며, 시프로플록사신, 레보플록사신, 목시플록사신 등 퀴놀론 계열 항생제는 DNA 합성에 필요한 국소이성화효소의 작용을 억제한다.
- 세포대사 억제 : 사람과 달리 세균은 필수적인 영양소인 엽산을 합성하기 위해 파라아미노벤조산을 필요로 한다. 술폰아미드 약물은 파라아미노벤조산을 엽산으로 전환하는 데 관여하는 효소의 경쟁적 억제제로 작용하여 정균작용을 나타낸다. 트리메소프림/술파메톡사졸의 조합이 대표적이다.
- 세포막 변경·파괴 : 폴리믹신 B와 콜리스틴은 세균의 세포막 투과성을 변화시킴으로써 살균작용을 나타낸다.
진핵세포와 항생물질[편집]
많은 항생제는 진핵세포 생물에게도 작용할 수 있다. 이러한 항생제는 곰팡이로 인한 질병 또는 암에 대해 강력한 효과를 발휘할 수 있으나, 사람 또한 진핵세포 생물이므로 이 항생제에 의해 피해를 입을 수 있다. 항암성 항생제에 대해서는 화학요법계열의 안트라사이클린 항목을 참고하기 바란다.
의의[편집]
항생제는 인류의 의학 기술과 평균 수명을 비약적으로 향상시킨 발명품이다. 과학이 지금처럼 비약적인 발전을 이루기 이전의 의술계에서는 병의 원인을 과학적 근거로 증명해 내지 못했기에 관념적이고 형이상학적인 미신적 이론으로 설명하였다. '장기설'이라 불리는, 나쁜 공기에서 병이 생긴다는 현대 기준에서 주장하면 진짜 못 배워먹은 소리 취급받을 이론이 정론으로 통하던 시절이었으니 말 다 했다. 그래도 주거 환경과 신체를 청결하게 하고, 감염병이 창궐할 시 환자가 쓰던 물건은 불태우는 등 기초적인 예방 지식 정도는 있었지만, 결국 병이 생겼을 때 근본적인 치료를 하지는 못했으니 완벽한 해답은 아니었다.
물론 이는 당시 과학 기술이 발달하지 못했기에 감염병을 일으키는 세균이나 바이러스 등의 병원체를 관찰해 내는 것이 불가능했기에, 그러한 병원체에 대한 개념조차 생각할 수 없었기 때문이다. 이는 초기 현대의학 역시 마찬가지였다. 산업혁명에 이어 일어난 과학혁명 이후 유럽의 로베르트 코흐, 루이 파스퇴르 등에 의해 드디어 세균학의 시대가 열렸고 이와 연관되어 화학, 생리학 그리고 현대의학이 발전하며 항생제 발견의 과학적 밑거름이 되었다. 이 발전에 힘입어 인류 역사상 최초로 1928년 8월 영국의 의학자 알렉산더 플레밍이 페니실린이라는 항생 물질을 발견한 이후 수억 명이 과학 발전의 혜택으로 목숨을 구할 수 있게 되었다.
항생제가 현대의학에 도입되기 이전에는 엄청난 수의 사람들이 지금 기준으로는 매우 사소한 감염 질환으로 죽어나갔다. 폐렴, 결핵, 연부조직 감염(봉와직염), 종기, 세균성 설사, 패혈증 등이 대표적. 과거에는 영유아뿐만 아니라 산모의 생존률도 많이 낮았는데, 출산하다가 세균 감염이 발생해 산욕열이 발병하면 손도 못써보고 산모가 죽는 경우가 많았기 때문이었다. 한국사에도 등창, 다시 말해 겨우 등에 난 종기 때문에 왕조차도 여럿 죽어나가던 시절이 있었다. 확 와닿게 말하면, 현재 기준으로는 연고나 빨간약만 있으면 되는 사소한 상처 하나로 인해 환부 절단, 심지어는 사망 직행이었던 시절이 불과 100년 전이다.
항생제 남용으로 인해 항생제 내성균의 발생이 증가하고 그로 인해 어떠한 항생제로도 치료가 불가능한 소위 '슈퍼박테리아'가 인류의 생존을 위협할 것이라는 우려가 있다. 실제로 항생제가 의학에 도입된 이후 새로운 내성균이 발생하고 있으며 세계보건기구도 이를 우려하고 있다. 하지만 이런 내성획득병원균은 대부분 독성이 강한 경우는 드물고 또한 만성질환자, 장기간 병원에 입원한 노인이나 면역결핍증 같은 환자들에 문제가 되지 정상적인 사람에겐 큰 문제를 일으키지 않는다.
일부 돌팔이들은 이를 근거로 '항생제는 무조건 나쁘므로 절대 쓰면 안 된다'라는 식의 주장을 하는데, '불필요한 항생제 사용은 지양해야 한다'라고 받아들여야지 비전문가들이 유사과학을 들이대는 걸 그대로 믿으면 안 된다.
사망 위험성이 있는 심각한 세균 질환, 대표적으로 세균성 폐렴이나 신우신염과 같은 경우에는 초기에는 주사제로, 조금 호전이 된다면 복용 약물로 변경하는 경우가 있다. 이때, 세균의 종류와 감수성(약물에 대한 취약성)을 확인하기 위해 혈액에서 세균 배양을 하지만, 이것이 꽤나 시간이 걸리는 관계로 '경험적' 항생제를 사용한다. 감염 부위, 증상 양상에 따라 가장 치료 확률이 높은 약물을 먼저 사용하고, 며칠 보면서 증상이 가라앉지 않는다면 2차 약물로 변경을 한다. 사실 혈액 배양은 다양한 시도에도 효과가 없을 때를 위한 보루라고 보면 된다. 세균성 감염이라면 경험적 치료로 95%는 호전되니까.
의사 중 일부는 항생제의 개발과 그 사용법의 정립이 현대의학 최대의 쾌거라고 보기도 한다. 당장 항생제가 없었더라면 발생했을 대표적인 일들은
- 수술 이후 감염으로 인한 사망률 급증
- 치과 발치 시 사망률 급증
- 매독, 임질, 클라미디아 등 각종 세균성 성병 창궐, 해결 방안 없음
- 말라리아 감염으로 인한 사망률 폭증
- 결핵 창궐
- 노인의 사망 요인 1위로 폐렴 등극
- 이질, 콜레라 등 세균성 설사 창궐
- 병사들의 환부 감염으로 인한 사지절단률 급증
- 피부 혹은 피하감염으로 인한 사망률 급증
이 외에도 수도 없이 많다.
항생물질에 대한 내성[편집]
항생제는 자연적으로 존재하던 것이었으므로, 이에 대한 저항성이 있을 것이란 것은 쉽게 예측 가능하다. 현재는 항생제 내성이 있는 미생물이 매우 많다. 이러한 미생물을 내성균이라 하며, 병의 치료 및 원내 감염이라고 불리는 상황에서 어려움을 주고 있다.
내성균의 비율은 자연적으로는 그리 많지 않았다. 그러나 페니실린의 개발 후 많은 사용에 따라 내성균의 비율이 크게 증가하였고, 이에 따라 페니실린만이 아닌 메티실린 등의 다른 항생물질이 필요하게 되었다. 또, 대체 항생물질에 내성을 가지는 슈퍼 박테리아가 발생되어 그 위험이 많이 증가하고 있다.
항생제 남용[편집]
- 항생제 사용에 첫 번째 규칙은 그것을 사용하지 않는 것이고, 두 번째 규칙은 되도록 이면 그것들을 많이 사용하지 않는 것이다.
- Paul L. Marino
부적절한 항생제 처방과 항생제의 과용은 항생제 내성 균들의 출현을 가속시켰다. 의료 지식을 갖추지 못한 일반인들 스스로가 처방하는 것과 농업에서 성장 촉진제로서 항생제를 사용하는 것은 더욱 더 문제를 악화시켰다.
더욱이 항생제는 그 사용상의 안정성이 보장되지 못한 상태에서 종종 처방되기도 하며, 때로는 환자에 맞지 않는 약이 처방될 때도 있다. 몇몇 경우에서는 굳이 항생제를 사용할 필요가 없는 상황에서도 처방되기도 한다. 1950년대에 들어서면서, 기적의 치료약으로 불리던 페니실린(penicillin)과 에리스로마이신(erythromycin)에 대한 내성이 모습을 드러냈다. 병원에서 치료 목적으로 광범위하게 항생제를 사용한 것 역시 다양한 항생제에 내성을 가진 세균(antibiotic-resistant bacteria)들이 등장하는 데에 일조했다.
여행자들이 예방 목적으로 사용하는 항생제를 포함하여 항생제를 오용하고 있는 경우는 대개 환자의 몸무게와 이전에 환자가 사용한 항생제들을 고려하지 못한 데에서 비롯한다. 두 변수 모두 항생제 처방 효과에 중대한 영향을 미치기 때문이다. 다른 오용의 경우, 처방자가 내린 투약 지시를 정확하게 따르지 않아 생기는데, 예를 들어 8시간마다 복용한다고 할 때 그냥 하루에 세 번 투약하는 것을 들 수 있다. 또 처방된 약을 끝까지 다 복용하지 않고, 중간에 투약을 중단하는 것도 문제가 된다. 이러한 습관은 항생제 내성 세균의 등장을 가속한다. 부적절한 처방 역시 문제가 된다. 그 대표적인 예로, 일반적인 감기와 같은 바이러스 감염으로 인한 질환에 아무 효과 없는 항생제를 사용하는 것이다. 호흡계 감염성 질환에 대한 한 연구는 의사들이 항생제 처방을 원하는 환자에게 더 많은 항생제 처방을 한다고 발표했다. 처방 받은 환자들 4명 중 1명 만이 실제적으로 항생제가 필요한 환자였다고 한다. 다원적인 항생제 사용 감시 체제는 오남용을 막기 위해 환자와 의사 모두에게 적용된다.
다양한 연관 기구들이 규제 풍조의 강화를 위한 로비 활동을 하고 있다. 미국에서는 항생제의 오남용에 대한 지속적인 관심 촉구를 위해 항생제 내성 대비 통합 테스크 포스 (Integracy Task Force on Antimicrobial Resistance)팀이 만들어졌으며 미국 질병 예방 관리 본부(US Centers for Disease Control and Prevention)와 식약청(FDA), 국립 보건원(NIH)와 협력하고 있다. NGO 단체들도 꾸준히 캠페인 활동을 하고 있다. 프랑스에서는 “항생제는 만병통치약이 아닙니다.”(“Antibiotics are not automatic”)라는 캠페인이 2002년에 시작되어, 불필요한 항생제의 사용을 획기적으로 줄였다. 영국의 병원 진료소에는 NHS가 제작한 포스터가 붙어 있는데 ‘항생제는 당신의 감기를 낫게 할 수 없을 겁니다’ 라고 쓰여있다. 이것은 바이러스 감염에 항생제를 처방해야 된다는 환자들의 무지를 일깨워 주는데 도움이 되었다. 대한민국에서는 법원이 항생제의 과 처방 병원 명단을 공개하라는 판결을 내려 항생제 오남용의 비율이 상당히 줄어들었으며 국민들의 인식도 크게 개선되었다.
동물의 성장 촉진제로서 항생제를 사용하여 결국 항생제 내성 균이 발생함에 따라 1970년 영국에서는 그것을 금지시켰다.(Swann report 1969). 현재 유럽 연합은 광범위하게 성장 촉진제로서의 항생제 사용을 금지하고 있다. 미국에서는 70% 이상의 항생제가 병이 없는 가축(소, 돼지, 닭)에게 사료와 함께 투여되는 것으로 추정된다. 가축에 사용된 항생제는 Salmonella spp, Campylobacter spp, Escherichia coli and Enterococcus spp 등의 내성 균주들의 출현에 기여했다. 미국과 유럽에서 나온 연구 결과에 따르면 이렇게 발생한 내성 균주들이 인간을 감염시킬 수 있으며, 기존에 처방 되던 항생제로는 치료가 불가능하다고 한다. 이런 문제들 때문에 일부 조직들 (The American Society for Microbiology (ASM), American Public Health Association (APHA) and the American Medical Association (AMA))이 축산물을 포함한 비치료 목적의 항생제 사용의 금지를 요청하고 있다. 하지만 법제화에는 몇 가지 이해관계에서 비롯된 난관이 존재하여 계속 미루어지고 있다. 특히 항생제를 파는 사업체들의 불만도 많으며 축산물에 대한 항생제 사용과 치료 불가능한 세균성 질병의 출현 사이의 직접적인 관계를 파악하는데 시간이 많이 걸린다. 대한민국에서도 가축용 사료에 대한 항생제 사용이 2011년 7월부터 전면 금지되었다.
항생제 대체 요법[편집]
다중 내성 세균의 처리법[편집]
다중 내성 세균(MDRO; Multi-drug-resistant organisms)이란 일반적으로 기존의 항생제 처방으로 죽일 수 없는 세균을 의미한다. 이처럼 항생제가 무용지물이 되는 상황이 발생하기 때문에 항생제를 대체할 수 있는 방법이 필요하다.
내성-변조 약물[편집]
내성-변조 약물(RESISTANCE MODIFYING AGENTS)에 대한 설명이다. 내성균에 맞서는 한 가지 방법으로 근래에 개발되고 있는 기술 중 하나는 다음과 같은 원리에 근거한다. 다중 내성 세균 자체를 약물학적인 방법을 통해 다시 항생제에 영향을 받도록 하는 것이다. 일반적으로 아래의 것들이 이러한 약물의 목표가 되고 있다.
- Efflux inhibition; Efflux mechanism-세균이 외부물질을 체외로 배설하는 메커니즘이다. Efflux inhibition은 이 Efflux 메커니즘을 방해해 항생제가 세균 바깥으로 빠져나가는 것을 막는다.
- Beta-Lactamase inhibitors; Beta-Lactamase는 페니실린과 같은 Beta-lactam계열의 항생제들을 소화시키는 효소이다. 이 효소를 억제 하므로 인해 다시금 세균은 Beta-lactam 계열의 항생제에 감수성을 나타내게 된다.
파지 테라피[편집]
세균을 감염시킬 수 있는 바이러스인 파지를 이용하는 방법이 파지 테라피(Phage Therapy)이다. 파지는 세균에게 있어서 생태학적 동반자인데, 다양한 환경에 존재하는 세균의 개체 수를 통제해주는 역할을 한다. 이 치료법은 1920년대 미국과 동·서 유럽에서 인간에게 실제로 사용되었다. 이 때의 성공적인 치료는 사실 일회적인 것이었다. 신약의 효용성을 판단하는데 사용되는 엄격한 과학적 연구에서는 파지 테라피가 매우 제한적이라는 결론이 났다. 1940년대 페니실린이 발견된 이후, 미국과 유럽은 파지 테라피에 대한 연구를 포기했다. 그리고 세균 감염에 대한 대책으로 항생제 개발에 박차를 가했다. 하지만 구 소비에트 연방은 연구를 계속했고, 그루지야의 Eliava Institute of Bacteriophage, Microbiology & Virology에서 연구를 이어나갔다. 내성균의 등장에 따라, 다시금 서방 의학계에서는 파지 테라피에 대한 관심이 나타났다. 연구는 아직도 진행 중인데, 영국의 Intralytix, Novolytics, 인도의 Gangagen와 같은 회사와 대학 그리고 미국과 유럽의 다양한 재단이 파지 테라피에 대해 연구하고 있다. 하지만 유전자 변형에 대한 문제 때문에 연구에 제한이 가해지는 것이 걸림돌이 되고 있다. 아직까지 파지 테라피가 실재적인 효용을 가지기에는 많은 연구가 필요한 단계이다.
박테리오신[편집]
박테리오신은 세균에 의해 생성되어 다른 세균에 작용하는 물질을 말한다. 저분자 항생제의 대체재로 각광받으며 특이적 수용체에 흡착함으로 작용한다. 1입자가 1개의 세균을 죽일정도의 높은 향균성을 지니기도 한다.
영양분 차단[편집]
영양분 차단은 항생제를 대체 할 수 있다. 철분 공급의 제한은 인체 내에서 세균의 급증을 막는 한가지 수단이다. 체내에서 철분을 빼내가는 메커니즘은 병원균 사이에서 거의 공통적이다. 이러한 것을 이용해서, 많은 연구진들이 철분을 제거하는 새로운 킬레이트제를 만들고 있다. 이 킬레이트는 다른 병원균들이 사용할 철분을 미리 없애버리는 것이다. 다만 균에만 작용하는 영양분 차단은 내성이 생길 수 있으며, 숙주 세포가 양분 부족으로 죽을 수도 있다는 리스크를 가지고 있다.
생균제[편집]
생균제(probiotics)는 항생제의 대체재로 살아있는 생균 등을 섭취하여 병원균과 경쟁을 시켜 수를 줄일 수 있게 한다.
항생제의 독성[편집]
항생제는 몸 속 미생물의 번식 및 작용을 억제하는 역할을 하기 때문에 몸에 유익한 미생물과 해로운 미생물의 작용을 구분하지 않고 억제한다. 이와 같은 항생제의 작용은 수많은 미생물들과 공존하는 인체 또는 동물에게 악영향을 줄 수 있다. 실제로 최근 밝혀진 바에 따르면 항생제 투여가 대장에 사는 유익한 세균인 유산균을 죽이고, 해로운 대장균의 작용을 촉진하여 대장염 등의 장 질환을 유발한다는 결과도 있다.
항생제의 분류와 목록[편집]
세포벽 합성방해[편집]
세균은 진핵세포와는 다르게 펩티도글리칸을 주 골격으로 하는 세포벽을 가짐으로써 대체적으로 저농도인 외부환경(hypotension)으로 인해 발생하는 높은 삼투압을 견딘다. 이때 세포벽 합성방해제를 주면 세포벽 합성이 잘 안 되면서 높은 삼투압을 버티지 못하고 세균이 파괴된다.
페니실린계[편집]
항생제라는 개념을 최초로 만들어낸 푸른곰팡이의 분비물을 추출해서 만드는 항생제. 포도상구균 배양 실험을 하던 알렉산더 플레밍이라는 과학자가 발견했다. 펩티도글리칸의 다당류 사슬을 서로 연결하는 데 관여하는 펩티드전달효소를 억제하는 작용 기전을 갖고 있다. 세포벽을 가진 세균들을 번식하지 못하게 세포벽의 합성을 원천적으로 방해하는 원리이기에 미코플라스마처럼 세포벽이 없는 세균에게는 효과가 없다.
- 1세대 페니실린 항생제(천연 페니실린)
- 벤질 페니실린
- 벤자딘 페니실린 - 주로 매독에 쓰는데 일반 의원급에서 맞을 수 있는 주사
- 페니실린V
- 페니실리네이스 내성 페니실린/항포도상구균 페니실린
- 메티실린(methicillin)
- 급성 간질성 신염(interstitial nephritis) 등 심각한 부작용으로 인해 지금은 사용되지 않는 항생제이다. 하지만 역사적으로 중요한 항생제 중 하나인데, 위에 서술한 것처럼 MRSA가 바로 이 항생제에 저항력을 가져 붙여진 이름이기 때문이다.
- 광범위 페니실린
- 2세대 페니실린 항생제
- 앰피실린(ampicllin) - 특히 리스테리아(Listeria) 및 장내구균(Enterococci)에 효과적으로 사용된다. 특히 2세대 페니실린 항생제의 경우, 포도상구균에 비효과적인데 만일 앰피실린과 Sulbactam이 혼합된 약물을 사용할 경우엔 포도상구균 역시 커버하게 된다. 영국 글락소스미스클라인(구 스미스클라인비참)에서 개발.
- 아목시실린(amoxicillin) - 페니실린 계열 중에서 현재 가장 대중적으로 사용되는 항생제이다. 소아에서는 보통 아목시실린+클라불란산칼륨을 7:1로 혼합한 형태로 사용(~네오시럽) 3.5:1로 혼합된 형태로도 사용가능(~듀오시럽) 성인에서는 375mg(아목시실린:클라불란산칼륨=2:1), 625mg(아목시실린:클라불란산칼륨=4:1)을 사용. 혼합된 약물을 사용할 시 포도상구균을 커버하게 된다. 영국 글락소스미스클라인(구 스미스클라인비참)에서 개발.
- 전체적으로 연쇄상구균 종류인 화농성연쇄상구균, 폐렴구균(Strep pneumoniae) 등에 효과적이나, 위에 서술한 것처럼 다른 약물과 혼합하지 않을 경우 포도상구균(Staphylococcus)엔 비효과적인 약물이다.
- 카복시페니실린계 (3세대 페니실린 항생제)
- 카르베니실린 (carbenicillin)
- 티카실린 (Ticarcillin) - 영국 글락소스미스클라인에서 개발
- 우레이도페니실린계(4세대 페니실린 항생제)
- 아즐로실린
- 메즐로실린
- 피페라실린(piperacillin) - 매우 광범위한 종류를 커버하는 항생제. 기본적으로 연쇄상구균(Streptococci) 등의 그람양성 박테리아와 대부분의 그람음성 박테리아 - 특히 Pseudomonas 까지 커버하게 된다. 하지만 이 약물만 사용할 경우엔 포도상구균(Staphylococci) 계열 박테리아에 비효과적이기 때문에 주로 Tazobactam이라는 β-lactamase 억제제와 혼합하여 사용한다. 이 혼합물을 zosyn, 혹은 tazocin 이라고 하는데 방금 서술한 것처럼 정말 대부분의 박테리아를 커버하기 때문에, 환자가 조금이라도 심각한 감염증상을 보일 경우, 이것과 반코마이신을 우선적으로 투여하는 경우가 상당수이다. 사실 의학적으로 보나 학술적으로 볼 경우, 박테리아의 민감도를 검사하여 그에 알맞은 항생제를 투여하는것이 옳은 방법이지만, 환자의 상태가 심각하여 치료를 지체할 여지가 없을 경우 등 특수한 경우에는 이 두 가지 약물만으로 치료를 시행하게 된다. 미국 화이자(구 레드리연구소)에서 개발.
- 베타-락타메이스 억제제
- 페니실린계 항생제는 베타-락탐고리라는 구조를 가지고 있는데, 항생제 내성균주 중에는 이 내성 고리를 부수는 효소를 분비하는 경우가 있다. 이런 효소들을 무력화시킴으로써 내성을 억제하는 역할을 한다.
- 클라불란산 (Clavulanic Acid) - 아목시실린 (합쳐서 amoxicillin/clavulanic acid/co-amoxiclav, Augmentin), 또는 티카실린 (ticarcillin/clavulanic acid, Timentin) 등이 있다. 이 중 오구멘틴(Augmentin) 등은 진통제로 만들기도 한다.
- 설박탐 (Sulbactam) - 암피실린/설박탐 (화이자 Unasyn)
- 타조박탐 (Tazobactam) - 피페라실린/타조박탐 (Zosyn, 화이자 타조신).
세팔로스포린계[편집]
세대가 내려갈수록 그람음성(gram negative) 박테리아를 더욱 효과적으로 커버하게 된다.
- 1세대 경구제 - Cephradine(세프라딘;브리스톨마이어스스퀴브 베로세프), Cefadroxil(세파드록실;브리스톨마이어스스퀴브 듀리세프), Cephalexin(대화 세파메칠), Cefatrizine(세프로), Cephapirin(세파피린)
- 1세대 주사제 - Cefazolin(세파졸린;아스텔라스 세파메진), Cephalotin(케푸린)
1세대 약물의 경우, 그람양성(gram positive) 박테리아를 커버하게 되며, 그 외 E. coli 및 Moraxella 등의 그람음성 박테리아를 커버한다.
- 2세대 경구제 - Cefaclor(세파클러, 릴리 시클러), Cefuroxime(국제 진세프 정, 글락소스미스클라인 알포린 주), Cefprozil(브리스톨마이어스스퀴브 세프질, 건일 세프로질)
- 2세대 주사제 - Cefamandole(세파만돌;릴리 만돌), Cefotiam(세포티암;다케다 세라도란), Cefoxitin(세폭시틴), Ceftezole(세프테졸), Cefotetan(세포테탄;아스텔라스 야마테탄), Cefmetazole(세프메타졸;다이이찌산쿄 세프메타존),Cefbuperazone(도야마 토미포란, 국제 진페라존), Cefminox(세프미녹스)
- 1세대가 커버하는 박테리아 전부와 더불어 Haemophilus, Klebsiella, Citrobacter, Morganella 및 Proteus 등의 그람음성 박테리아까지 커버하게 된다.
- 3세대 경구제 - Cefixime(세픽심;슈프락스), Cefpodoxime(세프포독심;바난정), Cefdinir(세프디니르;옴니세프), Cefditoren(세프디토렌;메이액트), Ceftibuten(세프티부텐;세프템), Cefetamet(세페타메트;세페신정(세페타메트피복실)), Cefteram(세프테람), Cefcapene(세프카펜;후로목스정)
- 3세대 경구제 - Cefixime(세픽심;아스텔라스 슈프락스), Cefpodoxime(세프포독심; 다이이찌산쿄 바난정), Cefdinir(세프디니르;엘티엘 옴니세프), Cefditoren(세프디토렌;메이지 메이액트), Ceftibuten(세프티부텐;시오노기 세프템), Cefetamet(세페타메트;로슈 글로보세프, 유나이티드 세페신정(세페타메트피복실)), Cefteram(세프테람;도야마 토미론)
- 3세대 주사제 - Cefotaxime(세포탁심;사노피 크라포란), Ceftriaxone(세프트리악손;로슈 로세핀), Ceftizoxime(세피티족심;엘티엘 에포세린), Cefodizim(세포디짐), Cefmenoxim(세프메녹심), Cefpimizole(세프피미졸;라니세프), Ceftazidime(세프타지딤;글락소스미스클라인 포텀), Cefoperazone(세포페라존;화이자 설페라존, 국제 페라탐), Ceftazidime + avibactam(세프타지딤+아비박탐 합성;Avycaz, Zavicefta)
- 4세대 주사제 - Cefepime(세페핌;브리스톨아미어스스퀴브 맥스핌), Cefpirome(세프피롬)
- 특히 녹농균을 효과적으로 커버한다.
- 5세대 -Ceftobiprole(세프토비프롤;제프테라), Ceftaroline(세프타로린;테플라로), Ceftolozane(세프톨로잔)
카바페넴계[편집]
이 계열의 항생제는 베타락탐 분해효소 저해제 내성 장내 세균에 의한 감염증이 의심될 때 사용해보는 사실상 최후의 항생제다. 여기에까지 내성을 가진 세균이 등장하게 되면 답이 없는데, 실제로 그런 세균이 등장해 2017년부터 이슈가 되고 있다.
- 티에남 (이미페넴 + 실라스타틴, 엠에스디)
- 메로페넴 (메로펜주사, 유한)
- 이미페넴 (프리페넴(중외) 외 다수)
- 에르타페넴 (인반즈주사, 엠에스디)
- 광범위 항생제 중에 하나로 균동정이 어려운데 환자의 바이탈이 흔들리는 경우 사용해볼 수 있다. 반감기가 길어서 1일 1회 투약이 가능하며 거의 대부분의 Enterobacteriaceae와 혐기성균에는 유효하나 아시네토박터, 그람양성균이나 패니실린 내성 폐구균에는 다른 동일계열 악제에 비해 상대적으로 항균력이 떨어진다.
- 도리페넴(피니박스, 일동-시오노기)
- 일본 시오노기에서 신규개발된 카바페넴계 항생제로 요로계 복합감염과 복강내감염에서 유효성이 확인되었으며 녹농균에 대해서는 항균력이 메로페넴보다 우월한 것으로 확인되었다. 그러나 기계호흡 중인 중환자의 세균성 폐렴 환자에게 사망 위험을 증가시킨다는 FDA 승인내용 변경이 있었고 피니박스를 시오노기와의 계약 하에 도입한 일동제약은 도입 11년 만인 2019년에 시오노기와 재계약 없이 발매를 중지했다.
글라이코펩타이드[편집]
펩티드의 교차연결점의 D-Ala-D-Ala 아미노산에 결합하여 펩티도글리칸의 소단위의 펩티드 전달을 억제함. 청기독성, 신장독성, 아나필락시스가 나타날 수 있다.
단백질 합성억제제[편집]
아미노글라이코사이드[편집]
박테리아의 리보솜(ribosome) 중 30S와 결합하여 단백질 합성을 직접 억제하고 mRNA 의 miscoding을 유도하여 박테리아를 살균하는 항생제. 특히나 그람음성(gram negative) 박테리아인 E. coli, Pseudomonas, Klebsiella 등으로 인한 감염에 매우 효과적인 약물이다. 하지만 콩팥 및 귀(ototoxicity)에 심각한 부작용이 발생할 수 있기에 심각한 감염이 아닐 경우 잘 사용되지 않는다. 주로 패혈증(sepsis), 신우신염(pyelonephritis), 골수염(osteomyelitis) 등의 경우에 사용된다.
아미노글라이코사이드 계열 항생제는 그람양성균에 대한 살균력도 있어서 연고에도 자주 사용된다.
- 스트렙토마이신
- 카나마이신
- 네오마이신 (마데카솔케어 및 복합마데카솔 연고, 3중복합항생제연고, 질염치료질정, 안연고, 점안액 등)
- 젠타마이신 (쎄레스톤지 크림, 라벤다 크림 등)
- 하이그로마이신
- 아미카신
- 스펙티노마이신
- 시소마이신
테트라사이클린 계열[편집]
박테리아의 리보솜(ribosome) 중 30S와 결합하여 박테리아의 성장을 억제시키는 항생제. 특히 세포 내 박테리아(intracellular bacteria)를 커버하는 데 매우 효과적인 약물이다. 주로 클라미디아(chlamydia), 콜레라(cholera), 라임병(Lyme disease), 마이코플라즈마(Mycoplasma) 및 스피로헤타(Spirochetes) 등으로 인한 감염에 사용된다.
부작용으로 석회화 된 조직에 쌓이게 되는데, 이 때문에 특히 임산부 및 만 8세 이전의 소아기 환자에게 사용을 금하게 된다. 그 외에도 간이나 피부에 부작용이 발생하기도 한다. 또한 장기복용이나 단기 반복복용 시 치아가 누렇게 영구 변색될 수 있고 근위축과 광과민증 등의 부작용이 있다.
- 테트라사이클린
- 옥시테트라사이클린 (화이자 테라마이신)
- 디메틸클로로테트
- 라사이클린
- 독시사이클린
- 아래의 미노사이클린(상품명 미노씬, 미국 화이자(구 레드리연구소)에서 개발, 한국 한정으로 SK케미칼에서 판매)과 함께 국내에선 여드름 치료용 항생제로 흔히 처방된다.
- 미노사이클린
- 티게사이클린
매크로라이드계열[편집]
박테리아의 리보솜(ribosome) 중 50S의 23S rRNA에 결합하여 펩티드사슬의 신장을 억제하는(bacteriostatics) 항생제.
1차 효과는 정균.
매크로라이드 계열 항생제의 대표적인 부작용으로 심근재분극 장애가 있다. 심장근육은 전기적으로 흥분 수축하여 박동한 뒤 빨리 이완되어야 다시 수축하여 정상적으로 박동할 수있는데, 흥분 후 이완이 늦어지면 이완이 제대로 안 된 상태에서 다시 무리하게 수축해야해서 심전도가 꼬여버린다. 재수 없으면 중상이나 쇼크 등으로 목숨이 경각에 달한 중환자마냥 심근세동이 일어나서 순환부전으로 사망한다. 그래서 매크로라이드는 심근의 전기적 이완을 방해하는 약성이 있어서 선천적으로 심전도에 문제가 있는 사람에게는 거의 사용하지 않는다. 까딱하면 비명횡사하니까. 또한 이 계열의 항생제를 투여할 때는 정기적으로 심전도 검사를 해서 심박동에 이상징후가 있는지를 살피게 된다. 그 외에도 복통, 구토 및 담즙울혈 등의 부작용이 있다.
전체적으로 그람양성(gram positive) 박테리아를 효과적으로 커버하며, 그 외에도 Mycoplasma, Chlamydia 및 Legionella 등을 커버하기 때문에, 웬만한 감기 및 폐렴 증상이 보일 경우 가장 먼저 처방받는 항생제이다.
- 에리스로마이신(erythromycin) - 특히 QT 연장이 발생할 확률이 매우 높다. 미국 일라이 릴리에서 개발.
- 아지스로마이신(azithromycin) (화이자 지스로맥스, 또는 지맥스의 상품명이 더 유명. 체내 반감기가 길어서 하루 1알만 먹으면 되므로 자주 쓰이는 경구항생제 중 하나이다.)
- 클래리스로마이신(Clarithromycin) - 특히 위궤양의 주범인 헬리코박터균을 제거하는 데 매우 효과적이다. 애보트 클래리시드가 있음.
기타 항생제[편집]
- 퓨시드산
- 리네졸리드 - 그람양성균에 대해 반코마이신이 듣지 않을 때 써볼 수 있는 선택지. 이른바 VRE(vancomycin resistant Enterococci)라는 슈퍼 박테리아에게 효과가 있는 항생제이다. 리네졸리드의 경우는 강력한 항균작용을 보이는 만큼 함부로 써서는 안 되지만 면역이 떨어진 환자가 MRSA에 걸린 게 확실한 경우에는 생존과 직결되는 문제이므로 빠르게 사용해야 한다.
- 다만, 리네졸리드를 많이 사용하다보면 환자가 있는 환경에 리네졸리드 내성 생긴 균이 발생할 수 있다. 리네졸리드에 내성이 있는 원내감염 MRSA 폐렴이라도 발생하면 해당 병동의 입원환자들이 이런 약 저런 약 다 써봐도 줄줄이 골로 갈 수 있다. 이 때문에 리네졸리드를 함부로 쓰지 않는 것이다.
DNA/RNA합성 억제제[편집]
핵산의 합성을 억제하고 방해하는 방식으로 작용하는 계열.
퀴놀론계[편집]
박테리아의 DNA 생성 관련 효소인 Gyrase 및 Type II topoisomerase (Topoisomerase IV) 와 결합해 DNA 복제를 억제하여 박테리아를 제거하는 항생제이다. 특히 그람음성(gram negative) 박테리아인 슈도모나스(Pseudomonas), 대장균(E. coli), 프로테우스(Proteus), 레지오넬라(Legionella) 및 임균(Gonorrhea)에 매우 효과적이다. 또한 레보플록사신(levofloxacin)과 목시플록사신(moxifloxacin)의 경우, 그람양성(gram positive) 계열 박테리아까지 커버하기 때문에 매우 자주 사용되는 약물이다. 특히 목시플록사신은 혐기성(anaerobes)까지 커버한다고. 주로 요로감염증(UTI), 폐렴 및 감염성 설사에 자주 사용된다. 대부분의 다른 항생제와는 다르게 전합성이 가능하다. 플루오르화 이전의 1세대 퀴놀론계 항생제는 시장에서 퇴출된 관계로 2세대 이후는 모두 플루오르화가 이루어져 있으며 이로 인하여 플루오로퀴놀론계 항생제로 불리기도 한다.
하지만 구토, 어지러움증 등의 부작용이 있으며 신장(nephrotoxicity)에 무리를 주기도 한다. 또한 임산부에겐 사용할 수 없는 단점이 있다. 추가적으로, 소아나 청소년에서는 약물 복용과 관련된 근골격계 부작용이 나타날 수 있기 때문에 18세 미만 소아청소년의 퀴놀론계 항생제 투여는 금기된다. 특히 근골격계 부작용은 상당히 큰 후유증이 남을 위험이 있으므로 관련 증상이 나타난다 싶으면 바로 전문의와 상담해야 한다.
- 날리딕산 (나리디산)
- 오플록사신 (다이이찌산쿄 타리비드, 일동 에펙신 등)
- 레보플록사신 (다이이찌산쿄 크라비트)
- 목시플록사신 (바이엘의 아벨록스라는 제품명으로 더 유명하다. 가장 최신 세대의 퀴놀론계 항생제로 강력하지만 그만큼 심부전의 부작용 확률도 높아진 게 단점.)
- 트로반
- 발로플록사신 (JW중외 큐록신)
리팜피신[편집]
- 리파마이신
- 리팜피신 (상기의 항생제를 화학적으로 합성한 제재. 결핵약에 대표적으로 쓰인다. 이탈리아 레펫티트에서 리파딘이라는 상품명으로 출시(한국에서는 한때 국제약품에서 판매), 현재 한국 한정으로 유한 리팜핀, 종근당 리포덱스가 있음.)
- 리팍시민
- 리파마이신 계열 항생제의 한 종류로, 이탈리아 Alfa Wasserman 에서 Normix라는 이름으로 개발, 시판했으며 한국에는 삼오제약-한올바이오파마에서 동명(노르믹스 정)으로 수입 제품을 발매 중이다. 승인받은 적응증은 세균감염에 의한 설사증후군(장내세균상 이상으로 인한 하계설사, 여행자설사, 소장결장염), 위장관수술 전후 감염의 예방, 고암모니아혈증의 보조요법이다. 니푸록사자이드 같은 다른 살균성정장제와 같이 체내에 흡수되지 않는 특성이 있다. 최근에 이 약을 여행자설사증후군의 예방 목적 및 과민성대장증후군 증후의 치료에 적용하는 시도가 계속되고 있으며 일부에서는 성공적이라는 견해가 있으나 이 역시 항생제이므로 예방 목적으로 함부로 사용하는 것은 좋지 못하다는 견해도 있다.
세포막 파괸제[편집]
원형질막에 결합하여 막구조와 투수성을 파괴한다. 협범위 마이코박테리아에 활성.
- 폴리믹신A
- 폴리믹신B
- 폴리믹신C
- 폴리믹신D
- 폴리믹신E(=Colistin)
- 암포테리신B계열 (항진균제에 포함된다. 길리어드 암비솜)
기타물질 합성방해제[편집]
- 설파제(Sulfa Drugs)- 술폰아미드 계열 성분을 사용한다. (이미 없어진 약품인 프론토실[19] 등을 포함한다.) 2차대전 등의 매체에서 가루 형태의 뿌리는 약으로 묘사되며, PABA의 경쟁적 억제제로 작용하여 엽산 합성 효소에서 엽산 합성을 저해한다. 원핵세포의 경우 엽산(Vit B9)을 자가합성할 수 있는 능력을 가진다. 이는 다음과 같은 과정을 거치는데: pterin+PABA-> DHP(엽산) (DHP synthase 촉매), DHP(엽산)->THP (DHP reductase 촉매), 이 중 원핵세포에서만 독보적으로 DHP synthase 촉매를 통한 DHP 합성 과정이 있기에 이를 억제하는 원리이다. 인간은 DHP(엽산)의 형태로 섭취하거나, 장내 세균의 합성을 통해 확보하기에, DHP synthase를 사용하지 않기에 영향을 받지 않는다.
현재 한국에서는 사용이 어려운 항생제[편집]
유럽이나 미국 등 다른 국가에서는 항생제 내성균으로 인하여 새롭게 개발된 항생제들이 있으나, 내성균에 최종적으로 쓸 수 있는 최신 항생제가 국내에 도입되어 있지 않아 중증 감염병 치료에 차질이 빚어지고 있다.
국내에서는 항생제 내성균 비율이 높음에도 도입이 이루어지지 않아 꼭 써야 할 대안 항생제를 못 쓰고 있지만 필요하다면 환자측이 최신 항생제를 희귀의약품센터에 요청해 비급여로 외국에서 사들여올 수 있다. 다만 비용도 문제일 뿐더러[20] 수입까지 최소 2~4주 걸린다. 이런 항균제가 필요할 정도로 치명적인 감염을 앓고 있는 환자들이 그런 시간을 기다릴수도 없을 뿐더러, 가격까지 고려하면 현실적으로 사용에 제약이 많을 수밖에 없다.
식약처 미허가[편집]
항생제(FDA 사용허가시기)
- 텔라반신(telavancin;2009년): 반코마이신 내성 장내 세균, 피부 연부조직 감염증
- 세프타롤린(ceftaroline;2010년): 항생제 무력화 효소 내는 장내 세균, 연쇄상구균과 메티실린 내성 포도상구균을 포함한 포도상구균, 지역사회 획득 폐렴(CAP) 원인균인 메티실린 감수성 포도상구균(MSSA) 및 폐렴 연쇄상구균
- 피닥소마이신(fidaxomicin;2011년): Clostridioides difficile 균의 감염증에 사용한다. 2021년부터 미국 감염학회는 해당 감염에 대해 이 약제를 가장 우선해서 사용하도록 권고하고 있다.
- Vabomere (2017; meropenem/vaborbactam): 다제내성 그람음성균의 치료에 사용한다.
식약처 허가[편집]
- 아비카즈(Avycaz;2015: 세프타지딤+아비박탐): 호기성 그람음성 세균감염증을 비롯한 원내폐렴, 복강내감염 및 요로감염, 민감성 미생물이 원인이 된 복잡성 복강내 감염증(cIAI)에 사용할 수 있다. 2022년 12월 22일자 식약처 사용 승인.
- 저박사 (zerbaxa;2015: ceftolozane/tazobactam): 다제내성 녹농균의 치료에 사용한다. 20년도 즈음 비보험으로 국내에서 사용되었으나 수입이 중단된 적이 있다. 2022년 10월 1일자로 급여 대상 포함.
참고자료[편집]
같이 보기[편집]

 위키원
위키원