"산화물 전고체 배터리"의 두 판 사이의 차이
(→상세) |
|||
| (다른 사용자 한 명의 중간 판 3개는 보이지 않습니다) | |||
| 1번째 줄: | 1번째 줄: | ||
| − | '''산화물 전고체 배터리'''는 무기 고체 전해질인 [[산화물]]을 사용한 '''[[전고체 배터리]]'''이다. 전고체 배터리 고체 전해질에는 또 다른 무기 고체 전해질인 황화물계와 유기 고체 전해질인 폴리머가 있다. 고체 전해질은 액체 전해질에 비해 이온전도도가 낮다는 것이 단점이다. 때문에 전고체 배터리가 상용화 되려면 소재 연구가 가장 우선이다. 이 가운데 황화물계 전해질의 전도도와 셀 성능이 우수한 것으로 평가되고 있다. | + | '''산화물 전고체 배터리'''는 무기 고체 전해질인 [[산화물]]을 사용한 '''[[전고체 배터리]]'''이다. 전고체 배터리 고체 전해질에는 또 다른 무기 고체 전해질인 황화물계와 유기 고체 전해질인 폴리머가 있다. 고체 전해질은 액체 전해질에 비해 이온전도도가 낮다는 것이 단점이다. 때문에 전고체 배터리가 상용화 되려면 소재 연구가 가장 우선이다. 이 가운데 황화물계 전해질의 전도도와 셀 성능이 우수한 것으로 평가되고 있다. 전고체 전지의 전해물 종류는 산화물, 황화물, 폴리머, 하이브리드로 구분되는데, 종류별로 보면 폴리머 65, 황화물 37, 산화물 21, 하이브리드 10 순으로 비중을 차지한다. 산화물계는 스타트업이 연구 중이다.<ref>경계영 기자, 〈[https://www.edaily.co.kr/news/read?newsId=02732246629052856&mediaCodeNo=257&OutLnkChk=Y "전고체, 2030년 배터리 시장 4%대로 올라설 전망"]〉, 《이데일리》, 2021-05-26</ref> |
{{자세히|전고체 배터리}} | {{자세히|전고체 배터리}} | ||
[[파일:액체전해질과 고체전해질 비교.png|썸네일|500픽셀|가운데|액체전해질과 고체전해질 비교]] | [[파일:액체전해질과 고체전해질 비교.png|썸네일|500픽셀|가운데|액체전해질과 고체전해질 비교]] | ||
| + | |||
| + | == 상세 == | ||
| + | * 전고체 배터리의 고체 전해질은 액체 전해질과 동등한 이온 전도도를 가져야 한다. 현행의 리튬 이온전지에 사용되고 있는 용매 전해질의 전기 전도도는 10⁻²S㎝⁻¹ 대이다. 이 값의 대부분은 전지의 동작과 관계되지 않는 음이온이 하전담체로 작용한 것이어서, 리튬이온 전도의 기여는 반 이하에 머무른다. 따라서 리튬이온 배터리를 전고체화 할 수 있는 고체 전해질의 이온 전도도는 10⁻³S㎝⁻¹ 정도이다. | ||
| + | * 리튬이온을 전도 종으로 10⁻³S㎝⁻¹ 이상의 이온 전도도를 나타내는 고체 전해질은 '''[[질화리튬]]'''이다. 그러나 이 물질은 안정인 전위 범위가 0.45V에 지나지 않고, 고전압의 전지를 구성하는데 장해가 된다. 그 후, 산화물계 재료에서도 1990년대에 나시콘형 결정 구조를 가지는 LiTi₂(P0₄)₃나 페로브스카이트형 구조의 Li₃xLa⅔-xTi0₃로 10⁻³S㎝⁻¹의 이온 전도도가 달성되었다. | ||
| + | * 이러한 재료 중에서 티탄의 원자가수는 +4 상태이지만 전이금속은 원자가수가 변화하기 쉬운 원소이다. LiTi₂(P0₄)₃에는 리튬 전극 기준으로 2.5V, Li₃xLa⅔-xTi0₃에서도 1.5V로 전자가 주입되어 d¹상태로 된다. 전지를 고전압화 해, 에너지 밀도를 높이기 위해서는, 음극에 낮은 전위를 나타내는 재료를 사용해야 하지만, 이러한 고체 전해질이 그러한 음극과 접촉하면 음극으로부터 주입된 d전자가 전자 전도를 가져오게 되어 전해질로는 작용하지 않는다. | ||
| + | :* 상기 물질은 내환원성이 낮기 때문에, 가닛(garnet)형 산화물계 고체 전해질을 고려할 수 있다. 즉 Li₇ La₃Zr₂0₁₂계의 이온 전도도는 거의 10⁻³S㎝⁻¹에 달했다. 그러나 높은 이온 전도도와 내환원성을 겸비하는 가닛형의 고체 전해질에도, 산화물계 재료에 공통의 해결해야 할 과제가 남아 있다. | ||
| + | :* 산화물계 고체 전해질의 경우, 결정격자 중의 리튬 확산은 매우 빠르다. 그러나 다결정의 세라믹은 입자 끼리나 계면(입계) 저항이 매우 높아진다. 또 리튬이온 이외의 원소도 확산을 시작해 활물질과 고체 전해질 중의 원소가 서로 만나서 계면에 반응상이 형성된다. | ||
| + | :* 그러나 '''[[붕산리튬]]'''(Li₃B0₃)을 사용하면 반응상의 형성을 억제할 수 있다. 이 물질의 이온 전도도는 10⁻⁶S㎝⁻¹에 지나지 않지만, 융점은 700℃로 매우 낮고, 저온에서 활물질과 접합하는 것이 가능하다. 즉 분리층과 작용하는 부분의 고체 전해질에는 고온 소결한 가닛형 산화물을 사용해, 그 위에 활물질과 붕산리튬의 혼합물을 저온으로 소결한 전극층을 형성한 것이 보고되고 있다. | ||
| + | |||
| + | == 산화물계 전해질 특성 == | ||
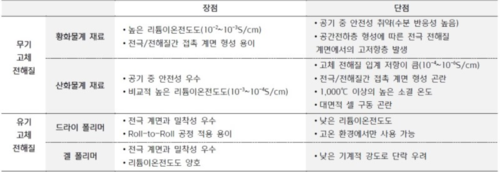
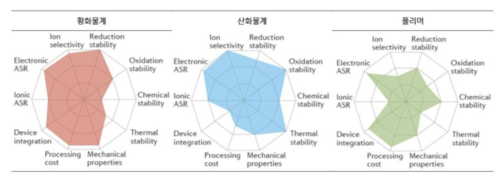
| + | 공기 중 안전성이 우수하고, 리튬 이온 전도도가 10⁻³~10⁻⁴ S/cm 수준으로 황화물계보다는 낮지만 비교적 높은 편이다. 전기화학적 안전성과 기계적 강도가 우수하고, 산화 전압이 높다. | ||
| + | |||
| + | 고체 전해질의 입계 저항이 크고, 전극과 전해질 간 접촉 계면 형성이 어렵다. 1,000℃ 이상의 고온 열처리 공정이 필요하고 셀을 대형화하기 어렵다. | ||
[[파일:고체 전해질의 종류별 장단점(전자부품연구원).png|썸네일|500픽셀|가운데|고체 전해질의 종류별 장단점(전자부품연구원)]] | [[파일:고체 전해질의 종류별 장단점(전자부품연구원).png|썸네일|500픽셀|가운데|고체 전해질의 종류별 장단점(전자부품연구원)]] | ||
| + | [[파일:고체 전해질 특성 비교.png|썸네일|500픽셀|가운데|고체 전해질 특성 비교]] | ||
| + | |||
| + | {{각주}} | ||
== 참고자료 == | == 참고자료 == | ||
* spainorange, 〈[https://blog.naver.com/hoonyang/221607951305 키움증권 차세대 배터리 - (3) Post Lib(전고체전지, 리튬황전지, 리튬공기전지 ]〉, 《네이버블로그》, 2019-08-06 | * spainorange, 〈[https://blog.naver.com/hoonyang/221607951305 키움증권 차세대 배터리 - (3) Post Lib(전고체전지, 리튬황전지, 리튬공기전지 ]〉, 《네이버블로그》, 2019-08-06 | ||
| + | * * 전고체 전지의 최신 기술기발(한국과학기술정보연구원) - file:///C:/Users/sms/Downloads/2._%EC%A0%84%EA%B3%A0%EC%B2%B4_%EB%A6%AC%ED%8A%AC%EC%9D%B4%EC%B0%A8%EC%A0%84%EC%A7%80_%EA%B0%9C%EB%B0%9C_%EB%8F%99%ED%96%A5_%EB%B0%8F_%EC%A0%84%EB%A7%9D.pdffile:///C:/Users/sms/Downloads/%EC%A0%84%EA%B3%A0%EC%B2%B4%20%EC%A0%84%EC%A7%80%EC%9D%98%20%EC%B5%9C%EC%8B%A0%20%EA%B8%B0%EC%88%A0%EA%B0%9C%EB%B0%9C.pdf | ||
| + | * 경계영 기자, 〈[https://www.edaily.co.kr/news/read?newsId=02732246629052856&mediaCodeNo=257&OutLnkChk=Y "전고체, 2030년 배터리 시장 4%대로 올라설 전망"]〉, 《이데일리》, 2021-05-26 | ||
== 같이 보기 == | == 같이 보기 == | ||
2023년 3월 9일 (목) 16:28 기준 최신판
산화물 전고체 배터리는 무기 고체 전해질인 산화물을 사용한 전고체 배터리이다. 전고체 배터리 고체 전해질에는 또 다른 무기 고체 전해질인 황화물계와 유기 고체 전해질인 폴리머가 있다. 고체 전해질은 액체 전해질에 비해 이온전도도가 낮다는 것이 단점이다. 때문에 전고체 배터리가 상용화 되려면 소재 연구가 가장 우선이다. 이 가운데 황화물계 전해질의 전도도와 셀 성능이 우수한 것으로 평가되고 있다. 전고체 전지의 전해물 종류는 산화물, 황화물, 폴리머, 하이브리드로 구분되는데, 종류별로 보면 폴리머 65, 황화물 37, 산화물 21, 하이브리드 10 순으로 비중을 차지한다. 산화물계는 스타트업이 연구 중이다.[1]
상세[편집]
- 전고체 배터리의 고체 전해질은 액체 전해질과 동등한 이온 전도도를 가져야 한다. 현행의 리튬 이온전지에 사용되고 있는 용매 전해질의 전기 전도도는 10⁻²S㎝⁻¹ 대이다. 이 값의 대부분은 전지의 동작과 관계되지 않는 음이온이 하전담체로 작용한 것이어서, 리튬이온 전도의 기여는 반 이하에 머무른다. 따라서 리튬이온 배터리를 전고체화 할 수 있는 고체 전해질의 이온 전도도는 10⁻³S㎝⁻¹ 정도이다.
- 리튬이온을 전도 종으로 10⁻³S㎝⁻¹ 이상의 이온 전도도를 나타내는 고체 전해질은 질화리튬이다. 그러나 이 물질은 안정인 전위 범위가 0.45V에 지나지 않고, 고전압의 전지를 구성하는데 장해가 된다. 그 후, 산화물계 재료에서도 1990년대에 나시콘형 결정 구조를 가지는 LiTi₂(P0₄)₃나 페로브스카이트형 구조의 Li₃xLa⅔-xTi0₃로 10⁻³S㎝⁻¹의 이온 전도도가 달성되었다.
- 이러한 재료 중에서 티탄의 원자가수는 +4 상태이지만 전이금속은 원자가수가 변화하기 쉬운 원소이다. LiTi₂(P0₄)₃에는 리튬 전극 기준으로 2.5V, Li₃xLa⅔-xTi0₃에서도 1.5V로 전자가 주입되어 d¹상태로 된다. 전지를 고전압화 해, 에너지 밀도를 높이기 위해서는, 음극에 낮은 전위를 나타내는 재료를 사용해야 하지만, 이러한 고체 전해질이 그러한 음극과 접촉하면 음극으로부터 주입된 d전자가 전자 전도를 가져오게 되어 전해질로는 작용하지 않는다.
- 상기 물질은 내환원성이 낮기 때문에, 가닛(garnet)형 산화물계 고체 전해질을 고려할 수 있다. 즉 Li₇ La₃Zr₂0₁₂계의 이온 전도도는 거의 10⁻³S㎝⁻¹에 달했다. 그러나 높은 이온 전도도와 내환원성을 겸비하는 가닛형의 고체 전해질에도, 산화물계 재료에 공통의 해결해야 할 과제가 남아 있다.
- 산화물계 고체 전해질의 경우, 결정격자 중의 리튬 확산은 매우 빠르다. 그러나 다결정의 세라믹은 입자 끼리나 계면(입계) 저항이 매우 높아진다. 또 리튬이온 이외의 원소도 확산을 시작해 활물질과 고체 전해질 중의 원소가 서로 만나서 계면에 반응상이 형성된다.
- 그러나 붕산리튬(Li₃B0₃)을 사용하면 반응상의 형성을 억제할 수 있다. 이 물질의 이온 전도도는 10⁻⁶S㎝⁻¹에 지나지 않지만, 융점은 700℃로 매우 낮고, 저온에서 활물질과 접합하는 것이 가능하다. 즉 분리층과 작용하는 부분의 고체 전해질에는 고온 소결한 가닛형 산화물을 사용해, 그 위에 활물질과 붕산리튬의 혼합물을 저온으로 소결한 전극층을 형성한 것이 보고되고 있다.
산화물계 전해질 특성[편집]
공기 중 안전성이 우수하고, 리튬 이온 전도도가 10⁻³~10⁻⁴ S/cm 수준으로 황화물계보다는 낮지만 비교적 높은 편이다. 전기화학적 안전성과 기계적 강도가 우수하고, 산화 전압이 높다.
고체 전해질의 입계 저항이 크고, 전극과 전해질 간 접촉 계면 형성이 어렵다. 1,000℃ 이상의 고온 열처리 공정이 필요하고 셀을 대형화하기 어렵다.
각주[편집]
- ↑ 경계영 기자, 〈"전고체, 2030년 배터리 시장 4%대로 올라설 전망"〉, 《이데일리》, 2021-05-26
참고자료[편집]
- spainorange, 〈키움증권 차세대 배터리 - (3) Post Lib(전고체전지, 리튬황전지, 리튬공기전지 〉, 《네이버블로그》, 2019-08-06
- * 전고체 전지의 최신 기술기발(한국과학기술정보연구원) - file:///C:/Users/sms/Downloads/2._%EC%A0%84%EA%B3%A0%EC%B2%B4_%EB%A6%AC%ED%8A%AC%EC%9D%B4%EC%B0%A8%EC%A0%84%EC%A7%80_%EA%B0%9C%EB%B0%9C_%EB%8F%99%ED%96%A5_%EB%B0%8F_%EC%A0%84%EB%A7%9D.pdffile:///C:/Users/sms/Downloads/%EC%A0%84%EA%B3%A0%EC%B2%B4%20%EC%A0%84%EC%A7%80%EC%9D%98%20%EC%B5%9C%EC%8B%A0%20%EA%B8%B0%EC%88%A0%EA%B0%9C%EB%B0%9C.pdf
- 경계영 기자, 〈"전고체, 2030년 배터리 시장 4%대로 올라설 전망"〉, 《이데일리》, 2021-05-26
같이 보기[편집]

 위키원
위키원