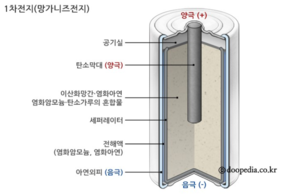
망가니즈전지(manganese battery)는 현재 가장 널리 이용되는 1차전지로, 프랑스의 조르주 르클랑셰가 고안하여 르클랑셰전지라고도 한다. 이산화망가니즈(MnO₂)를 양극 작용 물질, 아연(Zn)을 음극 작용 물질, 전해액을 염화 아연(ZnCl₂), 염화 암모늄(NH₄Cl) 등의 중성염 수용액으로 한 전지로 트랜지스터 라디오, 회중 전등 등에 널리 이용되고 있다. 또 tv리모콘이나 장난감, 시계 등 우리가 일반적으로 가장 많이 사용하고 있는 전지이다. 주로 전력소모가 적은 용도에 사용하고 있으며, 가격대 성능비가 우수해서 1차전지의 60%가량을 차지하고 있다.
개요
망가니즈전지는 대표적인 1차전지로 방전전압은 1.5V이며, 내부저항이 큰 단점이 있다. 음극에 아연, 양극에 탄소봉을 사용하고, 전해액으로는 염화암모늄과 염화아연의 혼합물을 사용하는 대표적인 1차전지이다. 일상적으로 사용하는 1.5V(볼트)의 건전지가 이것이다. 전해액이 넘쳐 흐르지 않도록 금속재질의 막대 모양으로 만든다. 내부저항이 커서오랜 시간연속으로 사용하기에는 적합하지 않다. 이전에는 자석식 전화기에 많이 사용하였고 다양한 소형전기제품에 사용한다.
발명
1868년 프랑스의 조르주 르클랑셰(Georges Leclanché, 1839~1882)는 망간산화물과 아연을 각각 양극과 음극으로 사용하고 전해액을 채워 전지를 구성했다. 이것이 현재의 아연-망간산화물전지(망간건전지)의 초기 작품이다. 초기에는 전해액이 수용액 상태인 습전지였으나, 1877년에 전해액을 석고 등으로 굳혀 액이 새지 않도록 해 마른 전지, 건전지를 만들었다. 망간건전지는 제조가 쉽고 안정성이 높으며 가격도 싸다. 주 재료인 이사화망간도 구하기 쉽다. 이런 이유로 망간건전지는 100년 이상 범용 전지로 사용됐다. 그러나 수명이 월등하게 긴 알칼리전지가 나오면서 차츰 빛이 바랬다. 망간건전지를 밀어낸 주인공은 알칼리전지다. 흔히 알카라인건전지라 부르는 것으로, 기존의 망간건전지와 동일한 물질을 사용한다. 단지 전해액으로 강 알칼리성 용액인 수산화칼륨용액을 사용하는 점이 망간건전지와 다르다.[1]
원리
음극 : Zn + 2NH₄Cl → [Zn(NH₃)₂]²⁺ + 2H⁺ + 2Cl⁻ + 2e⁻
양극 : MnO₂ + H⁺ + e⁻ → + MnO(OH)
양극 합제(合劑)는 이산화망가니즈(MnO₂)에 흑연 가루를 혼합하여 전기전도성을 좋게 한 것이다. 기전력은 1.5V이며, 방전량의 증가와 함께 전위도 서서히 저하하는 특성이 있다. 전압의 평탄성은 별로 좋지 않다. 에너지밀도는 20~50Wh/kg, 40~100W/l정도이다.[2]
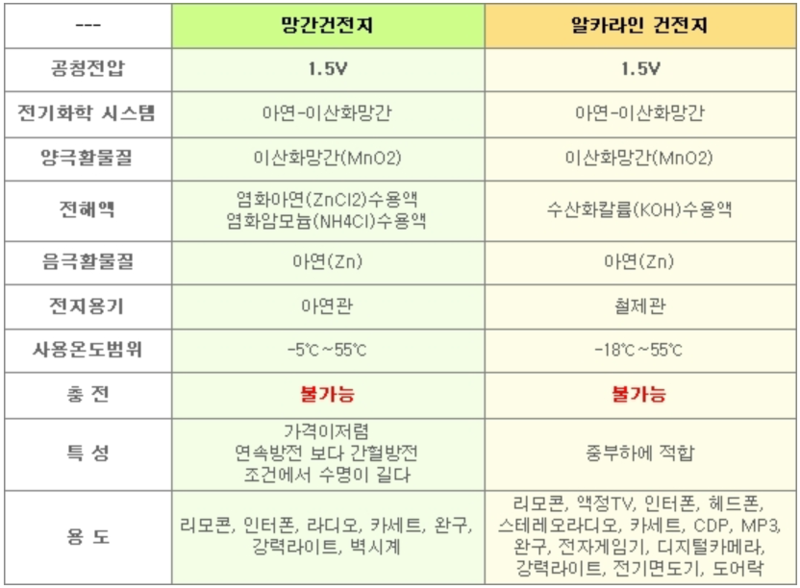
알칼리전지와 비교
각주
참고자료
같이 보기
|
  이 망가니즈전지 문서는 배터리에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요. 이 망가니즈전지 문서는 배터리에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요.
|
| 자동차 : 자동차 분류, 자동차 회사, 한국 자동차, 독일 자동차, 유럽 자동차, 미국 자동차, 중국 자동차, 일본 자동차, 전기자동차, 자동차 제조, 자동차 부품, 자동차 색상, 자동차 외장, 자동차 내장, 자동차 전장, 자동차 부품 회사, 배터리 □■⊕, 배터리 회사, 충전, 자동차 판매, 자동차 판매 회사, 자동차 관리, 자동차 역사, 자동차 인물
|
|
|
| 배터리 종류
|
1차전지 • 2차전지 • 3차전지 • AA 전지 • AAA 전지 • HFC • LCO • LFP • LMO • LTO • NCA • NCM • NCMA • 각형 배터리 • 건전지 • 고전압 배터리 • 고체전지 • 공기전지 • 과산화은전지 • 구반반 배터리 • 그래핀 배터리 • 금속 공기 배터리 • 나노셀룰로스 종이 배터리 • 나트륨이온 배터리 • 나트륨 황 배터리 • 납축전지 • 니켈 수소 배터리 • 니켈 카드뮴 배터리 • 다이아몬드 배터리 • 단추형 전지 • 대용량 배터리 • 대형배터리 • 동위원소 배터리 • 리튬공기전지 • 리튬 망간 배터리 • 리튬메탈 배터리 • 리튬 이산화탄소 배터리 • 리튬이온 배터리 • 리튬 인산철 배터리 • 리튬전지 • 리튬 코발트 배터리 • 리튬 티타네이트 배터리 • 리튬 폴리머 배터리 • 리튬 하이니켈 배터리 • 리튬 황 배터리 • 마그네슘 배터리 • 망가니즈전지 • 모래 배터리 • 무음극배터리 • 물리전지 • 미생물 연료전지 • 바나듐 배터리 • 바나듐 레독스 흐름 배터리 • 바나듐이온 배터리 • 바빌로니아 전지 • 박막배터리 • 박테리아 배터리 • 박테리아 종이 배터리 • 반고체 배터리 • 배터리 • 베타 배터리 • 보조배터리 • 볼타전지 • 불소이온 배터리 • 블레이드 배터리 • 비축전지 • 사원계 배터리 • 산화물 전고체 배터리 • 산화은전지 • 삼원계 배터리 • 설탕 배터리 • 세라믹 축전기 • 소금 배터리 • 소형배터리 • 수소연료전지 • 수은전지 • 슈퍼커패시터 • 습전지 • 아연공기전지 • 아연 탄소 전지(르클랑셰 전지) • 아폴로 • 알루미늄 공기전지 • 알루미늄 공기 흐름 전지 • 알칼리전지 • 얼티엄 배터리 • 에너지저장장치(ESS) • 에이터너스 • 연료전지 • 열전지 • 용융염 배터리 • 원자력전지 • 원통형 배터리 • 육둘둘 배터리 • 인섀시 배터리 • 전고체 배터리 • 전지 • 종이 배터리 • 중형배터리 • 차세대 배터리 • 초소형배터리 • 축전기(콘덴서) • 축전지 • 칼륨 배터리 • 칼슘 배터리 • 커패시터 • 코인셀 배터리 • 태양전지 • 파우치형 배터리 • 파워월 • 팔일일 배터리 • 폐배터리 • 폴리머 배터리 • 폴리머 전고체 배터리 • 프리폼 배터리 • 플렉서블 배터리 • 하이니켈 배터리 • 하이브리드 리튬메탈 배터리 • 해수전지 • 핵 배터리 • 화학전지 • 황화물 전고체 배터리 • 흐름전지(레독스 플로우 배터리)
|
|
|
| 배터리 기술
|
ALD • CCS • CSG • CTB • CTV • K-배터리 • MPI • MTB • NCMX • PCM • SRS • 건식분리막 • 계면 • 계면저항 • 계면활성제 • 고용량 • 고체전해질 • 고출력 • 공랭식 • 굴곡도 • 기공 • 기억효과(메모리 효과) • 냉각시스템 • 다공성 • 대용량 • 덴드라이트 • 드라이룸 • 모듈투바디(MTB) • 무기 고체 전해질 • 바인더 • 박막 • 박막화 • 방열판 • 방열핀 • 배터리관리시스템(BMS) • 배터리데이 • 배터리모듈 • 배터리 보호회로모듈 • 배터리셀 • 배터리 케이스 • 배터리 패키징 • 배터리팩 • 배터리하우징 • 배터리 히팅 시스템 • 복합전해질 • 분리막 • 블랙파우더 • 비전해질 • 사물배터리 • 산화물 • 산화물계 전해질 • 세라믹 코팅 • 세라믹 코팅 분리막 • 셀밸런싱 • 셀투바디(CTB) • 셀투비클(CTV) • 셀투섀시(CTC) • 셀투카(CTC) • 셀투팩(CTP) • 소용량 • 수랭식 • 스태킹 • 습식분리막 • 실리콘 음극재 • 실버코팅 • 안전성 강화 분리막(SRS) • 액체전해질 • 양극박 • 양극소재 • 양극재 • 양극판 • 양극활물질 • 여과 • 열폭주 • 열화현상 • 와인딩 • 용량 • 유기 고체 전해질 • 유랭식 • 음극소재 • 음극재 • 음극판 • 음극활물질 • 이온전달막 • 이온전도도 • 이온화 • 저용량 • 저출력 • 전고체 • 전구체 • 전지박 • 전해액 • 전해질 • 전해질막 • 점프 • 점프케이블 • 정격용량 • 정격전압 • 제로모듈 • 젤리롤 • 집전체 • 출력 • 침출 • 콤퍼레이터 • 티본 레이아웃 • 파우치 • 패스웨이 • 폐양극재 • 활물질 • 황화물 • 황화물계 전해질 • 히트싱크 • 히트파이프 • 히트펌프
|
|
|
| 배터리 제품
|
1865 배터리 • 2170 배터리 • 4680 배터리 • 기린 배터리
|
|
|
| 위키 : 자동차, 교통, 지역, 지도, 산업, 기업, 단체, 업무, 생활, 쇼핑, 블록체인, 암호화폐, 인공지능, 개발, 인물, 행사, 일반
|
|

 위키원
위키원