|
|
| 21번째 줄: |
21번째 줄: |
| | * [[아세틸렌]] | | * [[아세틸렌]] |
| | | | |
| − | {{배터리|검토 필요}} | + | {{화합물|검토 필요}} |
2022년 1월 26일 (수) 20:54 판
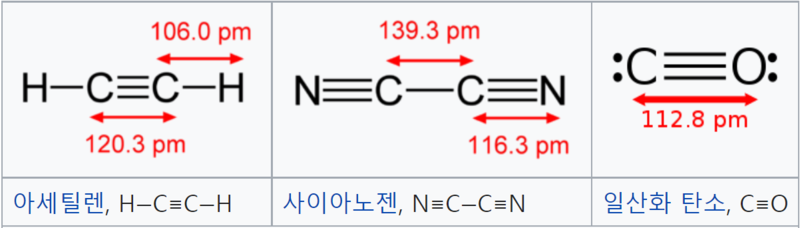
삼중결합(三重結合, triple bond)은 유기 화합물 분자 중에서 두 원자가 세 공유결합으로 이어져 있는 화학결합을 말한다. C≡C, C≡N, N≡N 등. 탄소 원자간의 삼중결합은 아세틸렌 결합이라 한다. 삼중결합은 본질적으로는 σ결합 1개와 π결합 2개로 구성되어 있다. 이들 2개의 π결합 때문에 삼중결합이 된 곳에서는 불포화성을 보여 첨가반응이 일어나기 쉽고, 또 산화 그 밖의 반응에 의하여 분자가 끊어지기 쉽다. 3중 결합에서는 이중 결합의 여러 특성이 다시 강한 모양으로 나타난다.
상세
두 원자 사이의 결합이 3개의 원자가결합을 나타내는 것으로, 하나는 σ결합이고 다른 2개는 그보다 전자구름의 겹침이 적은 π결합이다. 아세틸렌에서 볼 수 있는 HC≡CH가 대표적인 경우이다.
흔히 탄소·질소 등의 사이에서 볼 수 있는데, -C≡C-, -C≡N, N≡N과 같이 3개의 선, 또는 3개의 점으로 나타낸다. 이들 중에서 아세틸렌에서 볼 수 있는 HC≡CH은 대표적인 삼중결합이며, 아세틸렌결합이라고 한다. 삼중결합에 함유되어 있는 3개의 원자가결합은 서로 값이 같은 것이 아니라, 하나는 σ결합(σ전자에 의한 결합)으로 단결합의 경우와 같으나, 다른 2개는 그보다 전자구름의 겹침이 적은 π결합(π전자에 의한 결합)이다.
따라서 아세틸렌결합의 에너지는 133kcal/mol로, 단결합인 경우의 59kcal/mol의 3배보다는 적다. 이들 2개의 π결합 때문에 삼중결합이 된 곳에서는 불포화성을 보여 첨가반응이 일어나기 쉬우며, 또 산화 그밖의 반응에 의하여 분자가 끊어지기 쉽다.
삼중결합 화합물
참고자료
같이 보기
|
  이 삼중결합 문서는 원소에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요. 이 삼중결합 문서는 원소에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요.
|
| 산업 : 산업, 산업혁명, 기술, 제조, 기계, 전자제품, 반도체, 건설, 유통, 서비스, 에너지, 전기, 소재, 원소 □■⊕, 환경, 직업, 화폐, 금융, 금융사, 부동산, 부동산 거래, 부동산 정책, 아파트, 건물, 토지
|
|
|
| 원소
|
갈륨 • 경수소 • 구리 • 규소 • 금 • 금속 • 금속이온 • 나트륨(소듐) • 나트륨이온 • 납 • 네오디뮴 • 네온 • 니켈 • 동소체 • 동위원소 • 라돈 • 라듐 • 란타넘 • 란타넘족 • 루비듐 • 루테늄 • 리튬 • 리튬메탈 • 리튬이온 • 마그네슘 • 망가니즈(망간) • 바나듐 • 바나듐이온 • 방사성 동위원소 • 백금 • 베릴륨 • 붕소 • 브로민 • 비소 • 비철금속 • 사마륨 • 산소 • 삼중수소 • 세슘 • 셀레늄 • 수소 • 수소이온 • 수은 • 스칸듐 • 아르곤 • 아연 • 아연이온 • 아이오딘(요오드) • 악티늄 • 악티늄족 • 안정 동위원소 • 알루미늄 • 염소 • 오가네손 • 우라늄 • 원소 • 원자 • 은 • 인 • 저마늄(게르마늄) • 전이금속 • 전이후금속 • 제논 • 족 • 주기 • 주기율표 • 주석 • 준금속 • 중금속 • 중수소 • 지르코늄 • 질소 • 철 • 초우라늄 • 카드뮴 • 칼륨(포타슘) • 칼슘 • 코발트 • 코페르니슘 • 크로뮴(크롬) • 크립톤 • 타이타늄(티타늄) • 탄소 • 탄소-14 • 텅스텐 • 토륨 • 팔라듐 • 플루오린 • 플루토늄 • 할로젠(할로겐) • 핵종 • 헬륨 • 헬륨3 • 황
|
|
|
| 화합물
|
LNO • pH • 강 • 강철 • 경수 • 고분자 • 공유결합 • 과산화수소 • 과산화은 • 그래핀 • 금속결합 • 금속산화물 • 뉴세라믹 • 단백질 • 단일결합 • 두랄루민 • 디메틸 카보네이트 • 리튬 니켈 산화물 • 리튬산화물 • 리튬인산철 • 리튬 코발트 산화물 • 리튬 티타늄 산화물 • 메탄올 • 메탈실리콘 • 메테인 • 무기화합물 • 무쇠(주철) • 무수수산화리튬 • 물 • 반응식 • 벤젠 • 분자 • 분자량 • 분자식 • 불소 • 불화리튬(플루오린화 리튬) • 불화수소 • 붕산리튬 • 뷰텐(부틸렌) • 비금속 • 산 • 산성 • 산화물 • 산화은 • 산화제 • 산화철 • 산화칼슘 • 산화코발트 • 삼중결합 • 삼중수 • 선철 • 설탕 • 세라믹 • 셀룰로이드 • 소금 • 수산화나트륨 • 수산화니켈 • 수산화리튬 • 수산화물 • 수산화아연 • 수산화이온 • 수산화칼륨 • 수산화칼슘 • 수산화코발트 • 수증기 • 순물질 • 순철 • 실리카(이산화규소) • 실리콘 (규소) • 실험식 • 아미노산 • 아세테이트 • 아세트산 • 아세틸렌 • 아이소프렌(이소프렌) • 아크릴로나이트릴 • 알칼리 • 알칼리성 • 알코올 • 암모니아 • 얼음 • 에탄올 • 에테인 • 에틸렌 • 에틸렌 카보네이트 • 연철 • 염 • 염기 • 염기성 • 염산 • 염화나트륨 • 염화마그네슘 • 염화비닐라이덴 • 염화수소 • 염화칼륨 • 염화칼슘 • 올레핀 • 옹스트롬 • 요소 • 요소수 • 유기화합물 • 유리탄소 (free carbon) • 유리탄소 (glassy carbon) • 이산화망가니즈 • 이산화탄소 • 이산화티타늄 • 이소부틸렌(아이소뷰텐) • 이오노머 • 이온결합 • 이중결합 • 인산 • 인산리튬 • 인산염 • 인산철 • 인조흑연 • 일산화탄소 • 전기화학반응 • 중수 • 증류수 • 질산 • 질산나트륨 • 질산염 • 질산칼륨 • 질화리튬 • 천연흑연 • 청동 • 카르빈 • 카보네이트(탄산염) • 카본블랙 • 탄산 • 탄산나트륨 • 탄산리튬 • 탄산에틸렌 • 탄산이온 • 탄산칼륨 • 탄산칼슘 • 탄소강 • 탄소나노튜브 • 탄소화합물 • 탄화규소 • 탄화수소 • 특수강 • 페놀 • 페라이트 • 페로브스카이트 • 폴리부틸렌 • 폴리아미드 • 풀러렌 • 프로포폴 • 프로필렌 • 하이니켈 • 합금 • 홑원소물질 • 화학 • 화학결합 • 화학반응 • 화학반응식 • 화학식 • 화합물 • 환원제 • 황동 • 황산 • 황산니켈 • 황산망간 • 황산코발트 • 황화리튬 • 황화물 • 흑린 • 흑연
|
|
|
| 위키 : 자동차, 교통, 지역, 지도, 산업, 기업, 단체, 업무, 생활, 쇼핑, 블록체인, 암호화폐, 인공지능, 개발, 인물, 행사, 일반
|
|

 위키원
위키원