|
|
| 44번째 줄: |
44번째 줄: |
| | * [[음이온]] | | * [[음이온]] |
| | | | |
| − | {{소재|검토 필요}} | + | {{화합물|검토 필요}} |
2022년 2월 9일 (수) 00:05 판
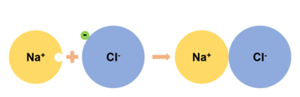
이온결합(ionic bond)은 화학결합의 한 형태로, 전하를 띤 양이온과 음이온 사이의 정전기적 인력에 기반을 둔 결합이다. 소금(염화소듐), 사파이어(산화알루미늄), 유리(산화규소)와 같이 주변에서 흔히 볼 수 있는 많은 물질이 모두 이온결합 화합물들이다.
개요
이온결합이란 금속과 비금속 이온 사이의 정전기 인력을 통한 화학 결합의 한 종류이다. 이온결합은 주로 전자가 많은 금속과 전자가 부족한 비금속 사이에서 일어난다. 금속은 전자를 잃어 양성자의 개수가 전자의 개수보다 많은 양이온이 되고, 비금속은 전자를 얻어 전자의 개수가 양성자의 개수보다 더 많은 음이온 상태가 된다.
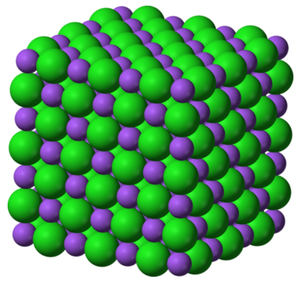
대표적인 이온결합 물질의 예로 염화나트륨을 들 수 있다. 염화나트륨은 이온 결합 결정으로 이루어진 고체로, 그림에서 보이듯이 일정한 규칙의 염소와 나트륨 이온들이 끊임없이 나열되어 있다. 이온 결합 물질인 소금은 양이온과 음이온이 서로 강하게 잡아당기는 결합을 하고 있기 때문에 녹는점이 높지만, 충격을 주면 양이온과 음이온 사이의 인력이 사라지며 쉽게 깨지게 된다.
원자가 껍질 (valence shell)에 전자가 거의 가득 차 있는 경우, 또는 전자가 거의 비어 있는 경우, 이 원자는 껍질을 완전히 채우거나 비우기 위해 매우 큰 반응성을 가질 수 있게 된다. 강하게 전기 음성도를 가진 원자는 종종 원자가 껍질에 하나 또는 두 개의 빈 궤도를 가지고 있으며 종종 다른 분자와 결합하거나 음이온을 형성하기 위해 전자를 얻으려고 한다. 전기 음성도가 약한 원자 (예를 들어 알칼리 금속)는 상대적으로 소수의 원자가 전자를 가지고 있기 때문에 전기 음성도가 강한 원자와 쉽게 공유 할 수 있다. 결과적으로 약한 음 전위 원자는 전자구름을 왜곡시키고 양이온 (cation)을 형성하는 경향이 있다.
이온결합의 특징으로는 상반된 전하를 띈 이온들 간의 전기적(쿨롱) 인력으로 서로 결합된 형태라는 것과 원소 간의 전기음성도 차이에 의해 이온결합 성향을 결정할 수 있다는 것이 있다. 또, 공유결합과 달리 방향성이 없어서 상하좌우 어디로나 양이온과 음이온이 번갈아 반복되는 구조를 갖는다. 마지막으로 물에 용해되면 이온결합이 끊어진다.
전기음성도(Electronegativity)는 원소가 전자를 끌어당기는 경향으로 이온결합을 하는 경향 정도를 나타내게 된다.
이온 화합물(Ionic Compound)는 이온결합에 의한 화합물을 일컬으며 전기적으로 중성을 띈다. 그의 예로는 할로겐 화합물이나 산화물이 있다. 이들은 대부분 고체 (이온결정) 형태를 띄고 금속과 비금속의 화학결합으로 생성되며 기본 구성 단위는 화학식 단위를 사용한다. 단원자 이온 화합물과 다원자 이온 화합물 (분자 이온; Molecular Ion)으로 분류된다.
특징
- 상반된 전하를 띈 이온들 간에 쿨롱(전기적) 인력으로 서로 결합된 형태
- 즉, 상하좌우 어디로나 양이온과 음이온이 번갈아 반복되는 구조[1]
각주
참고자료
같이 보기
|
  이 이온결합 문서는 원소에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요. 이 이온결합 문서는 원소에 관한 글로서 검토가 필요합니다. 위키 문서는 누구든지 자유롭게 편집할 수 있습니다. [편집]을 눌러 문서 내용을 검토·수정해 주세요.
|
| 산업 : 산업, 산업혁명, 기술, 제조, 기계, 전자제품, 정보통신, 반도체, 화학, 바이오, 건설, 유통, 서비스, 에너지, 전기, 소재, 원소 □■⊕, 환경, 직업, 화폐, 금융, 금융사, 부동산, 부동산 거래, 부동산 정책, 아파트, 건물, 토지
|
|
|
| 원소
|
갈륨 • 경수소 • 구리 • 규소 • 금 • 금속 • 금속이온 • 나트륨(소듐) • 나트륨이온 • 납 • 네오디뮴 • 네온 • 니켈 • 동소체 • 동위원소 • 라돈 • 라듐 • 란타넘 • 란타넘족 • 루비듐 • 루테늄 • 리튬 • 리튬메탈 • 리튬이온 • 마그네슘 • 망가니즈(망간) • 바나듐 • 바나듐이온 • 방사성 동위원소 • 백금 • 베릴륨 • 붕소 • 브로민 • 비소 • 비철금속 • 사마륨 • 산소 • 삼중수소 • 세슘 • 셀레늄 • 수소 • 수소이온 • 수은 • 스칸듐 • 아르곤 • 아연 • 아연이온 • 아이오딘(요오드) • 악티늄 • 악티늄족 • 안정 동위원소 • 알루미늄 • 염소 • 오가네손 • 우라늄 • 원소 • 원자 • 은 • 인 • 저마늄(게르마늄) • 전이금속 • 전이후금속 • 전형금속 • 제논 • 족 • 주기 • 주기율표 • 주석 • 준금속 • 중금속 • 중수소 • 지르코늄 • 질소 • 철 • 초우라늄 • 카드뮴 • 칼륨(포타슘) • 칼슘 • 코발트 • 코페르니슘 • 크로뮴(크롬) • 크립톤 • 타이타늄(티타늄) • 탄소 • 탄소-14 • 텅스텐 • 토륨 • 팔라듐 • 플루오린 • 플루토늄 • 할로젠(할로겐) • 핵종 • 헬륨 • 헬륨3 • 황
|
|
|
| 화합물
|
LNO • pH • 갈륨비소 • 강 • 강철 • 경수 • 고분자 • 공유결합 • 과산화수소 • 과산화은 • 그래핀 • 금속결합 • 금속산화물 • 뉴세라믹 • 단백질 • 단일결합 • 두랄루민 • 디메틸 카보네이트 • 리간드 • 리튬 니켈 산화물 • 리튬산화물 • 리튬인산철 • 리튬 코발트 산화물 • 리튬 티타늄 산화물 • 메탄올 • 메탈실리콘 • 메테인 • 무기화합물 • 무쇠(주철) • 무수수산화리튬 • 물 • 반응식 • 벤젠 • 분자 • 분자량 • 분자식 • 불소 • 불화리튬(플루오린화 리튬) • 불화수소 • 붕산리튬 • 뷰텐(부틸렌) • 비금속 • 산 • 산성 • 산화물 • 산화은 • 산화제 • 산화철 • 산화칼슘 • 산화코발트 • 삼중결합 • 삼중수 • 상대이온 • 선철 • 설탕 • 세라믹 • 셀룰로이드 • 소금 • 수산화나트륨 • 수산화니켈 • 수산화리튬 • 수산화물 • 수산화아연 • 수산화이온 • 수산화칼륨 • 수산화칼슘 • 수산화코발트 • 수소결합 • 수증기 • 순물질 • 순철 • 실리카(이산화규소) • 실리콘 (규소) • 실험식 • 아미노산 • 아세테이트 • 아세트산 • 아세틸렌 • 아이소프렌(이소프렌) • 아크릴로나이트릴 • 알칼리 • 알칼리성 • 알코올 • 암모니아 • 얼음 • 에탄올 • 에테인 • 에틸렌 • 에틸렌 카보네이트 • 연철 • 염 • 염기 • 염기성 • 염산 • 염화나트륨 • 염화마그네슘 • 염화비닐라이덴 • 염화수소 • 염화칼륨 • 염화칼슘 • 올레핀 • 옹스트롬 • 요소 • 요소수 • 유기화합물 • 유리탄소 (free carbon) • 유리탄소 (glassy carbon) • 이산화망가니즈 • 이산화탄소 • 이산화티타늄 • 이소부틸렌(아이소뷰텐) • 이오노머 • 이온결합 • 이중결합 • 인산 • 인산리튬 • 인산염 • 인산철 • 인조흑연 • 일산화탄소 • 전기화학반응 • 중수 • 증류수 • 질산 • 질산나트륨 • 질산염 • 질산칼륨 • 질화리튬 • 질화물 • 착이온 • 천연흑연 • 청동 • 초분자 • 카르빈 • 카보네이트(탄산염) • 카본블랙 • 킬레이트 • 탄산 • 탄산나트륨 • 탄산리튬 • 탄산에틸렌 • 탄산이온 • 탄산칼륨 • 탄산칼슘 • 탄소강 • 탄소나노튜브 • 탄소화합물 • 탄화규소 • 탄화수소 • 특수강 • 페놀 • 페라이트 • 페로브스카이트 • 폴리부틸렌 • 폴리아미드 • 풀러렌 • 프로포폴 • 프로필렌 • 하이니켈 • 합금 • 홑원소물질 • 화학 • 화학결합 • 화학반응 • 화학반응식 • 화학식 • 화합물 • 환원제 • 황동 • 황산 • 황산니켈 • 황산망간 • 황산코발트 • 황화리튬 • 황화물 • 흑린 • 흑연
|
|
|
| 위키 : 자동차, 교통, 지역, 지도, 산업, 기업, 단체, 업무, 생활, 쇼핑, 블록체인, 암호화폐, 인공지능, 개발, 인물, 행사, 일반
|
|

 위키원
위키원