수산화나트륨
수산화 나트륨(Sodium Hydroxide)은 수산화 이온과 나트륨 이온이 결합한 물질로 가성소다라고도 한다. 화학식은 NaOH이다. 물에 녹아 강염기성 수용액을 만든다. 식음료, 비누 등의 산업에서 널리 사용된다. 1998년에 세계적으로 4500만톤이 생산되었다. 화학 실험에서 가장 널리 사용되는 염기이다.
순수한 수산화 나트륨은 대기 중에서 수증기와 이산화탄소를 잘 흡수한다. 온도에 무관하게 물에 잘 녹으며 이 때 많은 열이 발생한다. 수산화칼륨은 잘 녹지 않는 에탄올과 메탄올에도 녹는다. 에테르나 다른 무극성 용매에는 녹일 수 없다. 수산화 나트륨 수용액은 섬유와 종이에 노란색 얼룩을 남긴다.
수산화나트륨은 강염기의 대표적인 물질로 다른 물질을 잘 부식시키는 위험한 물질이다. 단백질도 가수분해하기 때문에 손으로 직접 만지는 것은 좋지 않다. 수산화나트륨은 고체 결정 상태이기 때문에 화학 반응시에는 주로 물에 녹여 수용액을 만들어 사용하는데, 이때 많은 열을 발생시키므로 주의해야 한다. 만들어진 수용액을 산성용액과 반응시킬 때에도 많은 열을 발생하므로 묽게 하여 사용해야 한다.
1807년 험프리 데이비가 녹인 수산화나트륨(NaOH)을 전기분해하여 최초로 나트륨 원소를 만들었다. 나트륨은 가장 흔한 알칼리금속으로 물보다 가벼우며, 칼로 자를 수 있고 저온에서는 잘게 부서진다. 열과 전기를 잘 전도하고 광전효과가 크다. 물과 격렬하게 반응하여 수소를 발생시키며 수산화나트륨이 된다.
목차
개요
수산화나트륨(NaOH)은 흰색의 부식성, 알카리성 고체로서, 흡습성과 친수성 때문에 대기 중의 수분을 흡수하여 액화된다. 이 수산화나트륨은 공기 중의 CO₂를 빠른 속도로 흡수하므로 실험실에서 사용하는 수산화나트륨이 탄산나트륨으로 되는 것을 막기 위해서는 공기를 차단해야 한다. 이것은 가성소다, 소다잿물, 수산화나트륨으로 알려져 있고 수용성이며, 냄새가 없고, 비누와 같은 느낌이다. 또한, CAS 등록번호1310-73-2이고 분자량은 40.0이다.
제법
크게 나누어 전해법와 가성화법이 있다. 전해법은 염화나트륨 수용액을 전기 분해하고, 생성된 나트륨을 아말감으로 하여 염소와 분리하는 수은법과, 격막을 사용해서 염소를 분리하는 격막법이 있다. 가성화법에는 탄산나트륨 수용액을 석회유(石灰乳)로 처리하는 석회법과 탄산나트륨을 산화철(Ⅲ)과 용융한 후 이것을 뜨거운 물로 처리하는 산화철법이 있다
정제법
시판되는 수산화나트륨을 알데히드를 완전히 제거한 에탄올에 용해하고, 탄산염, 염화물, 규산염 등의 불순물을 걸러, 거른액을 농축해서 나트륨 에톡시드의 침전을 분리하고, 이것을 장시간 감압 가열해서 분해하면 고순도의 제품이 얻어진다. 위의 조작은 모두 이산화탄소를 제거한 공기 중에서 실시한다.
구조
결정은 특이한 이중층 구조(2매의 원자면이 층상 격자의 단위로 되어 있는 구조)로 Na⁺도 OH⁻도 5배위, 고온에서는 암염형 구조를 취한다.
물리적 성질
백색의 고체로 상온에서는 사방 결정계, 고온의 등축정 결계 β형과의 전이 온도는 299.6℃. 완전히 무수(無水)인 것은 녹는점 328℃이지만, 실제로는 물과 탄산염을 함유하기 때문에 녹는점 318.4℃, 끓는점 1390℃. d 2.130, n 1.3576. 용융열 1.70kcaL/moL, 생성열 102.7kcaL/moL. 자화율 χ -0.59×10⁻⁶e.m.u. 조해성이고 물에 녹기 쉽고, 그때 많은 열을 낸다. 용해열은 물 200moL에 대해 10.10kcaL/moL (18℃). 수용액은 강한 알칼리성. 용해도 물 0℃, 42g/100g ; 100℃, 347g/100g : 에탄올, 글리세롤에 쉽게 녹는다. 에테르, 아세톤, 액체 암모니아에 녹지 않는다.
화학적 성질
공기 중에서 수분 및 이산화탄소를 흡수하여 탄산염을 생성한다. 열에 대하여는 매우 안정되고, 강열하여도 물과 산화물로 분해되지 않는다. 플루오르와는 저온에서 반응해 플루오르화나트륨, 물 및 산소가 생기고, 염소, 브롬, 요오드와는 저온에서 여러 가지 옥시할로겐화물을 생성하지만, 고온에서는 할로겐화나트륨을 생성한다. 황과는 황화나트륨 및 티오황산나트륨을 생성한다. 셀렌과는 셀렌화나트륨과 아셀렌산나트륨을, 인과는 인화나트륨과 여러 가지 옥시인염을, 비소와는 아비산나트륨과 비소화수소를 생성한다.
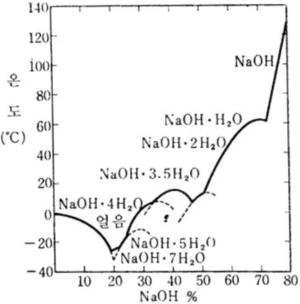
탄소와 강열하면 환원되어 나트륨이 생기고, 수소 및 일산화탄소를 발생한다. 칼슘도 적열 상태에서 나트륨이 생긴다. 용융염은 금 및 백금을 침해하고 규산염을 용해하기 때문에, 용융 수산화나트륨 처리에는 은 또는 니켈제의 도가니를 사용한다. 진한 수용액은 규소와 반응하여 규산나트륨 및 수소를 생성한다. 수용액은 강한 알칼리성으로 1, 2, 3, 3.5, 4, 5 및 7수화염이 존재하고, 이들의 용해도 곡선은 그림에 표시한 것과 같다.
수용액은 암모늄염에 작용하여 암모니아를 유리시키고, 또 대부분의 금속염 수용액에서 수산화물을 침전시킨다. 그러나 Pb, Sb, Sn, Al, Cr 및 Zn의 수산화물은 양쪽성이기 때문에 수산화나트륨을 더욱 과잉으로 넣으면 다시 용해된다. 규산염, 인산염, 황산염과 함께 용해하면 수용성의 나트륨염을 생성하기 때문에 분석상 알칼리 용융으로 불용성 염의 용해에 자주 사용된다. 일산화탄소와 반응해서 포름산나트륨을 생성하고, 유지를 비누화해서 지방산나트륨 및 글리세롤을 생성한다. 단백질, 셀룰로오스 등의 유기물을 분해하는 작용이 강하다.
용도
바이오디젤
바이오디젤을 생산할 때 수산화나트륨은 교환반응의 촉매로 사용된다. 물과 지방은 비누화반응을 일으키기 때문에 무수수산화나트륨만 이용할 수 있다. 더 싸고 적은 양이 필요하기 때문에 수산화칼륨에 비해 자주 쓰인다.
마약 제조
수산화나트륨은 메스암페타민이나 다른 마약을 제조하는데 필수적인 물질이다. 언론에 널리 알려진 것과 다르게 이것은 제조 원료로서 들어가는 것은 아니며 단지 화학 반응상 pH를 조절하기 위한 강염기로 사용되는 것이다.
산분해간장 제조
탈지대두에 염산을 섞어 고온에서 가수분해하여 아미노산을 생성시킨 뒤 수산화 나트륨으로 중화시키고 여과 및 정제를 거쳐 간장을 제조한다.
안정성
고체 수산화나트륨이나 고농도의 수산화나트륨 수용액은 심각한 수준의 화학적 화상을 유발할 수 있으며 영구적인 상흔이나 실명 등 인체에 부정적인 영향을 끼칠 수 있다.
알루미늄과 수산화 나트륨은 많은 수소 기체를 발생 시킨다.
2Al(s) + 6NaOH(aq) → 3H₂(g) + 2Na₃AlO₃(aq)
밀폐된 공간에서 수소 기체를 대량으로 발생시킬 경우 위험하다.
참고자료
- 수산화나트륨(전문연구위원 진영섭) - file:///C:/Users/sms/Downloads/%EC%88%98%EC%82%B0%ED%99%94%EB%82%98%ED%8A%B8%EB%A5%A8.pdf
- 〈수산화 나트륨〉, 《위키백과》
- 〈수산화나트륨〉, 《화학대사전》
같이 보기

 위키원
위키원