사마륨

사마륨(Samarium)은 화학 원소로 기호는 Sm, 원자 번호는 62이다. 단단한 은색의 금속으로 공기 중에서 쉽게 산화한다. 란타넘족의 전형적인 특성을 가지며, 주로 +3의 산화 상태를 가진다. 모든 산소족 원소들과 반응하여 화합물을 생성할 수 있다. 생물체 내에서는 중요한 역할 없이 약간의 독성을 띤다.
사마륨은 1879년 프랑스의 화학자 폴 에밀 르코크 부아보드랑이 발견하였다. '사마륨'이라는 이름은 원소가 발견된 '사마스카이트'라는 광물에서 유래하였다. 희토류 원소로 분류되기는 하지만 지각에는 40번째로 많은 원소이며 이는 주석보다도 더 흔하게 존재하는 것이다. 자연에서는 세라이트, 가돌리나이트, 사마스카이트, 모나자이트, 희토류광 등의 광물에 최대 2.8% 정도 포함되어있다. 이들 광물은 주로 중국, 미국, 브라질, 인도, 스리랑카, 호주 등에 많이 분포되어 있다.
또, 사마륨은 주로 네오디뮴 자석과 함께 강력한 자성을 가지는 사마륨-코발트 자석으로 쓰인다. 그러나 네오디뮴 자석은 조금만 가열해도 자성이 쉽게 사라지는데 반해 사마륨-코발트 자석은 약 700°C의 고온에서도 자성을 잃지 않는 성질이 있다. 방사성 동위 원소인 사마륨-153은 암 치료제로 사용되며 사마륨-149는 중성자를 잘 흡수하는 성질이 있으므로 원자로의 제어봉에 첨가된다. 화학 반응의 촉매, 방사능 연대 측정, X선 레이저 등에도 활용된다.
목차
개요
사마륨(samarium)은 원자번호 62번의 원소로, 원소기호는 Sm이다. 주기율표에서 란타넘족에 속하는 희토류 원소의 하나이다. 순수한 금속은 은색을 띠며, 란타넘족 원소 중에서는 가장 단단한 금속이다. 녹는점은 1072℃이고, 끓는점은 1794℃이며, 25℃에서 밀도는 7.52g/cm³이다. 다른 란타넘족 원소들과 마찬가지로, 화학 반응성이 크다. 화합물에서는 주로 +3의 산화상태를 가지나, 원자번호 63번의 유로품(Eu)과 마찬가지로, +2가 상태의 여러 화합물을 만들기도 한다. 공기 중에서 표면이 쉽게 산화사마륨(Sm₂O₃)으로 산화되어 노란색을 띠게 되며, 150℃이상에서는 자발적으로 불이 붙을 수 있다. 물과 반응하여 수산화사마륨(III)(Sm(OH)₃)이 되고 수소 기체를 발생시킨다. 산에 잘 녹아 수소를 발생시키고 Sm³⁺ 이온이 된다. Sm³⁺은 수용액에서 노란색의 [Sm(H₂O)₉]³⁺로 존재하며, Sm²⁺ 이온은 진한 붉은색을 띤다.
사마륨은 란타넘족 원소 중에서 세륨(Ce), 네오디뮴(Nd), 란타넘(La), 프라세오디뮴(Pr) 다음으로 지각에 많은 양이 존재한다. 지각에서의 존재비는 약 8ppm(0.0008%)으로, 대략 40번째로 풍부한 원소이며 모나자이트(monazite), 희토류광(bastnäsite), 세라이트(cerite), 가돌리나이트(gadolinite), 사마스카이트(samarskite) 등의 광석에 들어 있다. 사마스카이트 광석에서 처음 발견되었는데, 이 광석 이름은 이를 처음 발견한 사람의 이름 사마스키(Samarsky)에서 따왔고, 원소 이름은 광석의 이름에서 따왔다. 사마스카이트 광석의 화학적 조성은 (Y,Ce,U,Fe)₃(Nb,Ta,Ti)₅O₁₆로, 사마륨이 여기서 처음 발견되기는 했지만 함량은 조성에 표시되지 않을 정도로 적으며,현재 사마륨은 주로 모나자이트(사마륨 함량 2.7% 미만)와 희토류광에서 분리·생산된다. 흙에는 2~23ppm (1ppm = 1 x 10⁻⁴%), 그리고 바닷물에는 0.5~0.8ppt(1 ppt = 1 x 10⁻¹⁰%) 농도로 들어 있다. 전세계 연간 생산량은 산화사마륨(Sm₂O₃)으로 환산해서 약 700톤이며, 광석 매장량은 약 200만 톤으로 추정된다. 다른 희토류 원소들과 마찬가지로, 매장량은 많으나 분리하기가 어려워 생산량이 적으며 중국이 전세계 생산량의 약 95%를 차지한다.
사마륨의 가장 큰 용도는 코발트(Co)와 합금시켜 강한 영구자석을 만드는 것이다. 사마륨-코발트 자석은 보통 SmCo₅ 또는 Sm₂Co₁₇의 조성을 갖는데, 나중에 개발된 네오디뮴(Nd) 자석에 비해 값이 비싸고 자기장의 세기가 조금 약한 단점이 있으나, 높은 온도에서도 안정하고 잘 녹슬지 않는 장점이 있다. 사마륨 자석은 전기 모터, 헤드폰, 전기 기타(guitar)의 픽업(pickup, 소리나 빛, 진동을 전기적 신호로 변환시키는 장치) 등에 사용된다. 여러 사마륨 화합물들이 화학 반응의 촉매로 사용되며, 다이아이오드화사마륨(II)(SmI₂)는 유기 화학 반응에서 탄소-탄소 결합 형성의 짝지음제와 환원제로 널리 사용된다. 방사성 동위원소 ¹⁵³Sm은 방사성 암 치료제와 전이성 골암에 의한 뼈 통증 완화제로 사용되는 방사성 의약품의 주 성분이며, ¹⁴⁹Sm은 강한 중성자 흡수제로 원자로 제어봉에 첨가된다. 또한 다른 희토류 원소들처럼, 사마륨도 유리에 색을 내거나 적외선 흡수 유리와 같은 특수 광학 유리를 만드는데 쓰이며, 특수 용도의 레이저를 만드는데도 사용된다.
사마륨의 발견과 역사
사마륨은 19세기 후반에 여러 과학자들에 의해 검출되었다고 발표되었으나, 프랑스 화학자 부아보드랑(Paul Emile Lecoq de Boisbaudran, 1838~1912)이 1879년에 처음 발견한 것으로 인정받고 있다. 부아보드랑은 1879년에 미국 노스 캐롤라이나(North Carolina) 광산에서 채취된 사마스카이트 광석에서 얻은 디디뮴(didymium)의 산화물 디디미아(didymia)에서 새로운 금속 화합물을 분리하고, 여기서 나오는 스펙트럼 선의 관찰을 통해 새로운 원소인 사마륨을 발견하였다. 부아보드랑에 앞서, 1853년에 스위스 화학자 드 마리낙(Jean Charles Galissard de Marignac, 1817~1894)도 디디뮴에서 새로운 스펙트럼 선을 관찰하였으나 당시에는 새로운 원소나 화합물을 얻지 못하였는데, 부아보드랑보다 1년 늦은 1880년에야 가돌리늄(Gd, 원자번호 64)과 사마륨을 분리·확인하였다. 그는 이보다 2년 전에는 이터븀(Yb, 원자번호 70)도 발견하였다.
사마스카이트 광석은 1847년에 제정 러시아의 광산 공병단 참모장이었던 사마스키(Vasili Samarsky-Bykhovets, 1803~1870)에 의해 러시아 우랄 산맥 남부에서 처음 발견되었는데, 사마스키는 독일 광물학자 로제(Heinrich Rose, 1795~1864)에게 이 광석을 주어 연구하도록 하였으며, 로제는 이 광물을 사마스키의 이름을 따서 사마스카이트로 명명하였다. 부아보드랑은 그가 발견한 새로운 원소의 이름을 그 원소가 들어있던 광석의 이름인 사마스카이트를 따서 사마리아(samaria)로 정하였다. 그러나, 이 이름은 다른 희토류 금속 원소의 이름과 어미를 맞추기 위해 나중에 사마륨(samarium)으로 변경되었으며, 지금은 '사마리아'라는 말이 산화사마륨(Sm₂O₃)을 가리키는데 가끔 사용된다. 사마륨은 원소 이름을 사람 이름에서 따온 최초의 원소이다. 현재의 원소기호는 Sm인데, 1920년대까지는 Sa도 가끔 사용되었었다.
부아보드랑이 분리한 사마륨도 사실은 순수한 것은 아니었고 상당량의 불순물로 오염되어 있었다. 드마르세이(Eugene-Anatole Demarcay, 1852~1904)는 1896년에 스펙트럼을 통해 이 오염물질이 아직 알려지지 않은 새로운 원소일 것으로 짐작하였고, 1901년에는 이 새로운 원소인 유로퓸(Eu, 원자번호 63)을 분리∙발견함과 동시에 순수한 사마륨을 얻었다. 이온 교환방법으로 희토류 원소들을 분리하기 시작한 1950년대 이전까지는 사마륨이 순수한 형태로는 거의 사용되지 않았으며, 대부분 미시메탈(사마륨 함량 약 1%) 형태로 생산∙사용되거나, '사마륨-유로퓸-가돌리늄(SEG) 농축물' 형태로 생산되어 원자로의 중성자 제어봉에 사용되었다. 사마륨-코발트 자석은 1970년대 초반에 개발되어 사용되기 시작하였다.
물리직 성질
사마륨은 순수한 상태에서는 은색을 띠며, 굳기와 밀도는 아연(Zn)과 비슷한데, 희토류 원소들 중에서는 가장 단단하고 가장 부서지기 쉽다. 공기 중에서는 표면이 쉽게 산화되어 노란색을 띤다. 녹는점은 1072℃이고 끓는점은 1794℃인데, 란타넘족 원소 중에서는 끓는점이 이터븀(1196℃)과 유로퓸(1527℃) 다음으로 낮아 금속 사마륨을 증류 방법으로 분리하기도 한다. 25℃에서의 밀도는 7.52g/cm³이다. 실온에서는 삼방정(trigonal) 구조를 하는 α-형으로 존재하는데, 가열하면 731℃에서 육방조밀격자(hcp) 구조로 변하고, 더욱 가열하면 922℃에서 체심입방(bcc) 구조로 전환된다. 실온에서는 상자기성(paramagnetic)을 보이나, 온도를 내리면 14.8K에서 반강자성(antiferromagnetic: 원자의 전자 스핀이 인접한 스핀과 크기는 같으나 반대 방향으로 배열하여 순 자성이 0인 상태)으로 전환된다. 전기 비저항은 25℃에서 약 940nΩ∙m이다. 한편, 사마륨 원자를 플러렌(C60, 60개의 탄소 원자로 이루어진 축구공 모양의 탄소 동소체)에 캡슐화시키거나 플러렌 사이에 포함시킬 수 있는데 이렇게 생성된 물질은 8K이하에서 초전도 성질을 보인다. 또한 사마륨을 철을 기반으로 하는 초전도체에 첨가하면 초전도 전이온도가 56K까지 올라가는 것이 관찰되었다.
동위원소
사마륨은 천연상태에서 ¹⁴⁴Sm(3.07%), ¹⁴⁷Sm(14.99%), ¹⁴⁸Sm(11.24%), ¹⁴⁹Sm(13.82%), ¹⁵⁰Sm(7.38%), ¹⁵²Sm(26.75%), ¹⁵4Sm(22.75%)의 7 가지 동위원소로 존재한다. 이중 ¹⁴⁷Sm와 ¹⁴⁸Sm은 각각 반감기가 1.06x1011년과 7x1015년인 방사성 동위원소로 모두 α붕괴를 하고 ¹⁴⁷Sm은 ¹⁴Nd로, 그리고 ¹⁴⁸Sm은 ¹⁴⁴Nd가 된다. 따라서 천연 사마륨은 약한 방사능(128Bq/g)을 낸다. ¹⁴⁷Sm의 ¹⁴³Nd로의 α붕괴는 암석과 운석의 형성 연대를 결정하는 사마륨-네오디뮴 연대측정법에 이용된다.
질량수가 128~165 사이에 있는 많은 인공 방사성 동위원소들이 확인되었는데, 반감기가 긴 것들은 ¹⁴⁶Sm(반감기 1.08x108년), ¹⁵¹Sm(반감기 90년), ¹⁴⁵Sm(반감기 340 일), ¹⁵³Sm(반감기 46.3 시간), ¹⁵⁶Sm(반감기 9.4시간)이고, 나머지들은 반감기가 10분 이내이다. 질량수가 146보다 작은 동위원소들은 주로 전자포획(β+ 붕괴)을 하고 프로메튬(Pm) 동위원소가 되며, 질량수가 150보다 큰 동위원소들은 주로 β- 붕괴를 하고 유로퓸(Eu) 동위원소가 된다. ¹⁴⁶Sm은 α붕괴를 하고 ¹⁴²Nd가 된다.
¹⁴⁹Sm는 ²³⁵U보다 20배나 중성자를 잘 흡수하기 때문에 원자로의 제어봉에 사용되는데, 열 중성자에 의한 ²³⁵U의 핵분열 때도 자체 생성되어 전체 생성물의 1.0888%를 차지한다. 열중성자에 의한 ²³⁵U의 핵분열 때 ¹⁵¹Sm도 0.4203%의 수율로 생성되고 플루토늄-239(²³⁹Pu)의 핵분열에서는 보다 높은 수율로 생성되는데, 원자로 제어봉에 첨가되는 ¹⁴⁹Sm가 2개의 중성자를 포획하여 생성되기도 한다. ¹⁵¹Sm는 반감기가 90년으로 β- 붕괴를 하고 ¹⁵¹Eu가 되기도 하지만, 원자로에서는 대부분이 중성자를 포획하여 ¹⁵²Sm가 된다. 따라서 이들 사마륨 동위원소들의 생성과 소멸은 원자로를 설계하고 작동할 때 유념해야 할 중요한 인자가 된다. 한편, 인공 방사성 동위원소인 ¹⁵³Sm은 여러 암의 치료제와 전이성 골암 통증 완화제로 사용되는 방사성 의약품 Sm-¹⁵³ 렉시드로남(lexidronam)(상품명, 쿼드라메트(Quadramet))의 주성분으로, 핵 반응로에서 농축된 ¹⁵²Sm₂O₃에 중성자를 쪼여 ¹⁵³Sm₂O₃형태로 얻는다. 5가지 준안정한 핵 이성체들이 확인되었는데, 반감기가 긴 것들은 ¹⁴¹mSm(반감기 22.6분), ¹⁴³m¹Sm(반감기 66초), ¹³⁸mSm(반감기 10.7초)이다.
화학적 성질
사마륨은, 다른 란타넘족 금속 원소와 마찬가지로, 화학 반응성이 크다. 원자의 바닥 상태 전자배치는 [Xe]4f⁶6s²이며, 화합물에서 가장 흔한 산화 상태는 +3이다. 여러 +2 상태의 화합물들도 알려져 있는데, 산화물(SmO), 칼로겐화물(SmZ, Z=S, Se, Te), 할로겐화물(SmX₂: X=F, Cl, Br, I) 등이 있다. 특히 SmI₂는 유기화학 반응에서 탄소-탄소 결합 형성 반응의 짝지음제와 환원제로 널리 사용된다. 사마륨은 공기 중에서 쉽게 산화되어 표면이 노란색을 띠게 되며, 150 oC 이상에서는 자발적으로 불이 붙을 수 있다. 물과 반응하여 수산화사마륨(III)(Sm(OH)₃)이 되고 수소 기체를 발생시키며, 산에 잘 녹아 Sm³⁺ 이온이 되고 수소를 발생시킨다. Sm³⁺은 수용액에서 노란색의 [Sm(H₂O)9]³⁺로 존재하며, Sm²⁺ 이온은 진한 붉은색을 띤다. Sm³⁺의 표준 환원 전위 (Eo)는 다음과 같다.
- Sm³⁺ + e⁻ Sm²⁺ E ⁰ = -1.55 V
- Sm³⁺ + 3 e⁻ Sm E ⁰ = -2.30 V
즉 수용액에서 Sm³⁺는 안정하며, Sm²⁺는 강한 환원제로 작용한다.
한편, 사마륨 분말을 흑연(탄소), 인(P), 또는 비소(As)와 가열하면 각각 탄화사마륨(Sm₂C₃, SmC₂), 인화사마륨(SmP), 비소화사마륨(SmAs)을 만들 수 있는데, SmP는 띠 간격이 1.10eV인 n-형 반도체 성질을 보인다. 또한 사마륨 분말을 규소(Si), 저마늄(Ge), 주석(Sn), 납(Pb), 또는 안티모니(Sb)와 가열하면 대응하는 사마륨의 금속 합금들이 만들어지며, 산화사마륨(Sm₂O₃) 분말을 붕소(B)와 함께 진공에서 가열하면 여러 붕소화물들(SmBx: X=2, 4, 6, 66 등)이 만들어진다. 사마륨의 유기금속 화합물은 SmCl₃를 LiR 또는 NaR (R= 알킬 또는 아릴)와 반응시키면 얻을 수 있다.
- SmCl₃ + LiR → SmR₃ + 3 LiCl
사마륨의 생산
사마륨은 다른 희토류 원소들과 마찬가지로, 주로 모나자이트(monazite)와 희토류광(bastnäsite)에서 추출된다. 분쇄한 광석을 염산이나 황산으로 처리하면 희토류 금속 산화물은 수용성인 염화물이나 황산염으로 전환된다. 여과해서 얻은 산성 용액에 수산화소듐(NaOH)을 가해 토륨을 ThO₂로 침전시켜 제거하고, 여액을 옥살산암모늄((NH₄)₂C₂O₄)으로 처리하면 희토류 원소의 옥살산염이 침전으로 얻어진다. 이 염을 가열·분해시켜 혼합 산화물로 전환한다. 혼합 산화물을 염산에 녹여 혼합 염화물을 얻고, 이를 용융 상태에서 전기분해시키거나 칼슘(Ca)으로 환원시키면 희토류 금속 혼합물인 미시메탈(mischmetal)이 얻어지는데, 미시메탈에는 사마륨이 약 1% 들어 있다. 혼합산화물에서 란타넘(La), 세륨(Ce), 네오디뮴(Nd) 등 다른 용도가 많은 희토류 원소들을 분리시키고 나면 ‘린세이 혼합물(Lindsay Mix)’ 또는 SEG(사마륨-유로퓸-가돌리늄) 농축물이 얻어지는데, 이들 혼합물에는 붉은색 인광체로 사용되는 아주 값비싼 유로품(Eu)이 들어 있어, 유로퓸을 분리·생산하고 남은 부산물로 사마륨을 얻기도 한다. 순수한 사마륨은 희토류 혼합 산화물을 이온 교환 크로마토그래피나 용매 추출 방법을 사용하여 분리해서 얻는다.
사마륨은 주로 산화사마륨(III)(Sm₂O₃) 형태로 생산되어 판매된다. 금속 사마륨은 염화사마륨(III)(SmCl₃)를 염화소듐(NaCl) 또는 염화칼슘(CaCl2₂)과 함께 용융시켜 전기분해시키면 얻을 수 있으며, Sm₂O₃를 란타넘(La) 또는 바륨(Ba)으로 환원시킨 후 증류하여 얻을 수도 있다.
사마륨의 전세계 연간 생산량은 산화사마륨(III)(Sm₂O₃)으로 환산해서 약 700톤이며, 매장량은 약 200만 톤으로 추정된다. 다른 희토류 원소들과 마찬가지로, 중국에서 약 95%가 생산된다. 사마륨은 몇 가지 중요한 용도로 요긴하게 사용되고 있지만, 현재는 수요보다는 공급이 많은 편이어서 가격이 란타넘족 원소 중에서 가장 저렴한 편이다. 2012년 11월 현재 금속 사마륨(순도 99% 이상) 가격은 미화로 60$/Kg인데 4-7월에는 약 140$/kg이었으며, 산화사마륨(순도 99% 이상) 가격은 30$/kg이고 4-6월에는 약 90$/kg이었다. 희토류 원소의 수요와 가격이 국제 경기 상황에 따라 얼마나 민감하게 변하는가를 엿볼 수 있다.
사마륨의 용도
사마륨은 사마륨-코발트 영구자석, 화학 촉매와 시약, 방사성 의약품, 특수 유리 및 레이저 등에 사용된다.
영구자석
사마륨의 가장 큰 용도는 코발트와 합금시켜 강한 영구자석을 만드는 것이다. 사마륨-코발트 자석은 보통 SmCo₅ 또는 Sm₂ Co17의 조성을 갖는데, 현재까지 알려진 자석 중에서 가장 강력한 네오디뮴 자석(Nd₂ F₁₄B)에 비해 값싼 철 대신 값비싼 코발트를 사용하기 때문에 가격이 비싸고 자기장의 세기가 약간 작은 단점이 있다. 그러나 퀴리온도(Tc, 물질이 자석 성질(강자성)을 잃는 온도)가 높고(네오디뮴 자석은 310-400℃인데 비해, SmCo₅는 720℃이고 Sm₂ Co₁₇는 820℃), 잘 녹슬지 않으며, 온도에 따른 자기장의 세기 변화율이 적은(네오디뮴 자석의 약 1/4에 불과) 장점들이 있다. 사마륨-코발트 자석은 가격이 비싸기 때문에 소형 전기 모터, 헤드폰, 전기 기타(guitar)의 픽업 등 소형 용도로 사용되는데, 구체적인 예로는 태양 에너지를 이용한 경비행기인 솔라 챌린저(Solar Challenger)의 전기 모터, 사마륨 코발트 무잡음(Samarium Cobalt Noiseless: SCN) 전기 기타와 베이스(bass)의 픽업 등이 있다.
화학촉매와 시약
사마륨과 사마륨 화합물은 화학반응에서 촉매와 시약으로 널리 사용된다. 예로, 플라스틱의 분해 반응, 공해 물질의 하나인 폴리염화비페닐(polychlorinated biphenyl, PCB)의 탈염소화 반응에서 촉매로 사용된다. 또 에탄올을 비롯한 지방족 일차 알코올을 탈수소화시켜 알데하이드와 케톤으로 전환시키는데 산화사마륨(III)(Sm₂ O₃)이 촉매로 사용되며, Sm(III)의 트라이플루오르화메테인슬폰산염(samarium(III) trifluoromethanesulfonate, Sm(CF₃SO₃)₃: Sm(OTf)₃로 표기하기도 하며 samarium(III) triflate로 부르기도 함)은 가장 강력한 루이스산 촉매의 하나이다.
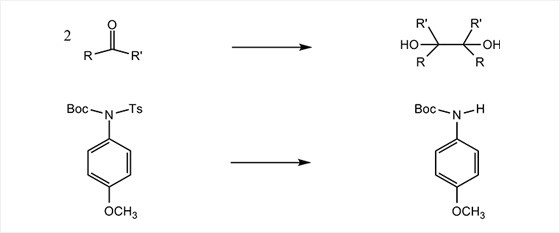
사마륨 화합물 중에서 가장 흔히 사용되는 것은 다이아이오드화사마륨(samarium diiodide, SmI₂ )이다, 이 화합물은 유기화학 반응에서 탄소-탄소 결합 형성 반응의 짝지음제(coupling agent)와 환원제 등으로 사용되는데, SmI₂ 를 이용한 반응의 예는 다음과 같다.
이와 같은 SmI₂를 사용하는 유기화학 반응은 의약품이나 천연물 합성에 중요하게 이용된다.
방사성 의약품
사마륨의 방사성 동위원소의 하나인 ¹⁵³Sm은 방사성 의약품에 사용된다. ¹⁵³Sm는 β-선을 방출하며 반감기는 46.3시간인데, 보통 에틸렌다이아민테트라메틸렌 포스페이트(ethylenediamine tetramethylene phosphate, EDTMP)와의 착화합물로 만들어 정맥주사제로 사용된다. 폐암, 전립선암, 유방암, 골육종(osteosarcoma)의 암세포를 죽이는 치료제로 사용되며, 전이성 골암에 의한 뼈 통증 완화제로 사용되기도 한다. 이 의약품은 Sm-153 렉시드로남(lexidronam)으로 불리며, 상품명은 쿼드라메트(Quadramet)인데, 1997년에 미국 식품의약국(FDA)에서 사용 승인을 받았다.
원자로 제어봉의 중성자 흡수제
¹⁴⁹Sm은 강한 중성자 흡수제로, 원자로 제어봉에 산화물 형태로 첨가된다. 초기에는 '린세이 혼합물(Lindsay Mix)'을 사용하였으나, 지금은 주로 SEG(사마륨-유로퓸-가돌리늄) 농축물 형태를 사용한다. 사마륨은 흔히 사용되는 붕소(B)나 카드뮴(Cd)에 비해 중성자 흡수 후의 생성물들도 좋은 중성자 흡수 성질을 보여 오래 동안 안정하게 사용될 수 있는 장점이 있다.
유리, 레이저, 기타 응용
산화사마륨(Sm₂ O₃)은 영화산업에서 촬영용 조명으로 사용되는 탄소 아크등 전극의 한 성분으로 사용되며, 유리의 노란색 착색제로도 사용된다. 사마륨이 첨가된 유리는 가장 값비싼 유리의 하나로, 주로 적외선을 흡수하는 특수 광학 유리로 사용되며, 400nm 이하의 빛을 흡수하므로 자외선 필터로도 사용된다. 사마륨 화합물은 적외선으로 들뜨는 인광체에 대한 감광제로도 사용된다.
사마륨은 여러 종류의 레이저에도 사용된다. 사마륨이 첨가된 플루오르화칼슘(CaF₂ ) 결정은 1961년에 만들어진 최초의 고체상태 레이저에서 활성 매질로 사용되었다. 또한 사마륨을 입힌 유리에 적외선 Nd:유리 레이저에서 나오는 펄스를 쪼여 생성시킨 사마륨 플라스마를 활성 매질로 하는 X-선 레이저도 제작되었는데, 이 레이저는 파장이 10nm보다 짧은 펄스를 발생시키기 때문에 홀로그래피, 고분해능 현미경 등 다양한 분야에 사용될 수 있다. 한편, 사마륨은 사마륨-네오디뮴 연대 측정법에 이용되기도 하는데, 이는 ¹⁴⁷Sm, ¹⁴⁴Nd, ¹⁴³Nd의 상대적 비로 암석이나 운석의 형성 기원과 연대를 결정하는 것이다.
모노칼로겐화사마륨(samarium monochalcogenide, SmZ, Z=S, Se, Te)은 실온에서 높은 압력을 가하면 반도체 상태에서 금속 상태로 전이가 일어나는데, 이런 성질을 이용하여 이들을 압력센서나 메모리 소자로 사용하는 장치가 개발되고 있다. 또 SmS는 가열하면 전위차가 생성되므로, 열-전기 변환장치에 이용될 수 있다.
생물학적 역할과 독성
성인의 몸에는 약 50μg의 사마륨이 주로 신장과 간에 들어있고 혈액에도 약 8μg/L의 농도로 녹아 있으나, 인체에서의 사마륨의 역할은 알려진 것이 없다. 사마륨이 대사를 촉진한다는 보고도 있으나, 이것이 사마륨에 의한 것인지 아니면 이에 포함된 다른 란타넘 원소에 의한 것인지는 분명하지 않다. 물에 녹지 않는 사마륨 염들은 독성이 없으나 물에 녹는 염들은 약한 독성을 보이는데, SmCl ₃의 쥐에 대한 치사량(LD50)은 복강 내 주사의 경우는 585mg/kg, 입으로 섭취한 경우는 2000mg/kg으로 보고되었다. 섭취된 사마륨 염의 약 0.05%만 혈액으로 흡수되고, 나머지는 배설되는 것으로 파악된다.
참고자료
같이 보기

 위키원
위키원